- Aufmerksamkeits- und Hemmungsstörungen, verstärkt durch Sedierung oder Schlaflosigkeit,
- Verlangsamung der Informationsverarbeitung,
- Reizbarkeit,
- motorische Unruhe,
- emotionale Dysregulation,
- Beeinträchtigung des Arbeitsgedächtnisses,
- Visusveränderungen,
- usw. (Campos-Castelló & Campos-Soler, 2004).
Größere Defizite finden sich bei pharmakoresistenten Patienten, besonders mit frühem Erkrankungsbeginn, da sie langjährige Chronizität und mehrere Therapien erleben.
Dosis und Anstiegsraten müssen beachtet werden, da kognitive Symptome dosisabhängig zunehmen.
6. Hirnplastizität
Die funktionelle Reorganisation in pädiatrischer Epilepsie zeigt, dass Sprache und Gedächtnis flexibel sind und sich während der Entwicklung verlagern können – etwa von der linken Dominanzregion ins rechte Hemisphären-Pendant oder zu nichttraditionellen Regionen (Brazdil et al., 2005). Dennoch ist dies individuell sehr komplex und erfordert spezialisierte neuropsychologische Rehabilitation.
Diese Faktoren unterscheiden sich je Patient. In Epilepsie sind subkortikale Funktionen (Aufrechterhaltung der Aufmerksamkeit, Arbeitsgedächtnis, Verarbeitungsgeschwindigkeit, kategoriales Abrufen) primär betroffen und verschlechtern sich durch Medikamente zusätzlich.
Klinische und neuropsychologische Manifestationen bei Epilepsie
Primär betroffen sind Aufmerksamkeit, Gedächtnis, Sprache, Verarbeitungsgeschwindigkeit, Hemmung und Arbeitsgedächtnis. Bei entwicklungsbedingten Enzephalopathien ist die Beeinträchtigung umfassender, sodass interdisziplinäre Teams erforderlich sind.
Die Symptomatik epileptischer Patienten ähnelt oft anderen Neuroentwicklungsstörungen. Daher können Rehabilitationsstrategien aus anderen klinischen Bereichen (kognitive Stimulation, Optimierung oder Kompensation) angewendet werden.
Wichtigster Aspekt in der Intervention ist die Semiotik des Anfalls und seine Entwicklung, da sie kognitives Profil und Verlauf bestimmen.
Epilepsie in anderen Pathologien
Epilepsie tritt auch bei zerebraler Kinderlähmung, genetischen Syndromen, Autismus etc. auf und verschlechtert dort klinische Manifestationen oder verursacht neuropsychologische Regressionen.
Jede wiederkehrende Anfallsform beeinträchtigt kognitive Funktionen, auch als benign geltende kindliche Anfälle. Zwar fehlen initial Symptome, langfristig zeigen sich subtile Defizite (Aufmerksamkeit, Arbeitsgedächtnis, Hemmung). Daher sind auch hier Diagnostik und Monitoring wichtig.
Anforderungen an ein neuropsychologisches Rehabilitationsprogramm bei Epilepsie
Ein neuropsychologisches Rehabilitationsprogramm sollte:
- Auf theoretische Bezugsmodelle zurückgreifen,
- eine interdisziplinäre Perspektive im Umfeld des Kindes (Therapie, Schule, Familie) annehmen,
- Prioritäten klar festlegen,
- Einsatz möglichst früh beginnen,
- ausreichend Therapiedauer (fallabhängig) garantieren,
- auf erhaltene Fähigkeiten aufbauen,
- Emotionale und motivationale Variablen berücksichtigen,
- starke Familienunterstützung einbinden.
Bedeutung der Neurorehabilitation bei Epilepsie
Neurorehabilitation ist nicht nur für kognitive Stimulation und Rehabilita-tion entscheidend, sondern auch, um das kognitive Profil und Anfallsmuster zu verfolgen.
Neuropsychologische Behandlung ermöglicht ein fortlaufendes klinisches Monitoring und schult den Neuropsychologen in der Semiotik einzelner Patienten. So lassen sich subtile klinische Veränderungen oder neue Muster in Anfallsverläufen erkennen, verursacht durch medikamentöse Anpassungen, emotionale Zustände oder Überstimulierung.
Dies erlaubt, kognitive Verschlechterungen oder Krankheitsprogression zu dokumentieren und medikamentöse Anpassungen zu empfehlen, um Nebenwirkungen zu minimieren.
Abschließend sei betont, dass alle Programme (digital oder Papier) lediglich Werkzeuge zur Förderung betroffener Prozesse sind. Erfolg hängt vom definierten Ziel und der Methodik ab.
Testen Sie NeuronUP 7 Tage kostenlos
Probieren Sie unsere verschiedenen Übungen, erstellen Sie Sitzungen oder arbeiten Sie remote mithilfe von Online-Sitzungen
Kognitive Prozesse sind nicht unabhängig, insbesondere bei netzwerkbasierten Störungen wie Epilepsie. Das menschliche kognitive System beruht auf der Interaktion verschiedener neuropsychologischer Prozesse, die sich in Entwicklung und Erholung gegenseitig beeinflussen. Daher ist es wichtig, keine isolierte Funktionsrehabilitation anzustreben.
Wenn Ihnen dieser Artikel zu Klinischer Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie gefallen hat, könnten Sie auch an folgenden Beiträgen interessiert sein:
Dieser Artikel wurde übersetzt; Link zum Originalartikel auf Spanisch:
Neuropsicología clínica en la neurocirugía de la epilepsia pediátrica
- Generalisierte Anfälle betreffen tiefe subcorticale Strukturen, Thalamus und retikuläres Formatio-System, die komplexe Funktionen steuern.
- Fokale Epilepsien sind oft mit spezifischen neuropsychologischen Defiziten je nach Anfallslokalisation verbunden (Mulas et al., 2006).
3. Anfallsfrequenz
Häufigere Anfälle beeinträchtigen kognitive Funktionen stärker.
4. Ätiologie oder Epilepsiesyndrom
Epileptische Enzephalopathien (z. B. West, Lennox-Gastaut) haben schlechteste Prognose mit progredienter Beeinträchtigung durch exzessive, diffuse elektrische Aktivität (Nieto, 2011).
5. Pharmakotherapie
Antiepileptika können durch Anfallskontrolle positive kognitive und emotionale Effekte haben, doch sie beeinflussen auch neuronale Netze, die Kognition regulieren, und können unerwünschte neuropsychologische Effekte verursachen.
Moderne Antiepileptika haben geringeren kognitiven Impact, doch zeigt sich in der Praxis weiter eine Beziehung zwischen Medikation und kognitiver Leistung. Beeinträchtigungen sind meist spezifisch und nicht generalisiert.
Monotherapie
Bei zu hohen Blutspiegeln oder rascher Dosissteigerung (Álvarez-Carriles et al., 2011) können auch zwei Medikamente mit geringem kognitiven Nebeneffekt kombinierte Probleme verursachen (Moog, 2009).
Die meisten Antiepileptika reduzieren Membranerregbarkeit, erhöhen postsynaptische Hemmung oder stören Netzsynchronisation. Dies verringert Verarbeitungs- und Aufmerksamkeitsgeschwindigkeit, was in sich entwickelnden Gehirnen stark einschränkend wirken kann.
Allgemeine Nebenwirkungen antiepileptischer Medikamente
Trotz individueller Unterschiede lassen sich folgende Nebenwirkungen festhalten:
- Aufmerksamkeits- und Hemmungsstörungen, verstärkt durch Sedierung oder Schlaflosigkeit,
- Verlangsamung der Informationsverarbeitung,
- Reizbarkeit,
- motorische Unruhe,
- emotionale Dysregulation,
- Beeinträchtigung des Arbeitsgedächtnisses,
- Visusveränderungen,
- usw. (Campos-Castelló & Campos-Soler, 2004).
Größere Defizite finden sich bei pharmakoresistenten Patienten, besonders mit frühem Erkrankungsbeginn, da sie langjährige Chronizität und mehrere Therapien erleben.
Dosis und Anstiegsraten müssen beachtet werden, da kognitive Symptome dosisabhängig zunehmen.
6. Hirnplastizität
Die funktionelle Reorganisation in pädiatrischer Epilepsie zeigt, dass Sprache und Gedächtnis flexibel sind und sich während der Entwicklung verlagern können – etwa von der linken Dominanzregion ins rechte Hemisphären-Pendant oder zu nichttraditionellen Regionen (Brazdil et al., 2005). Dennoch ist dies individuell sehr komplex und erfordert spezialisierte neuropsychologische Rehabilitation.
Diese Faktoren unterscheiden sich je Patient. In Epilepsie sind subkortikale Funktionen (Aufrechterhaltung der Aufmerksamkeit, Arbeitsgedächtnis, Verarbeitungsgeschwindigkeit, kategoriales Abrufen) primär betroffen und verschlechtern sich durch Medikamente zusätzlich.
Klinische und neuropsychologische Manifestationen bei Epilepsie
Primär betroffen sind Aufmerksamkeit, Gedächtnis, Sprache, Verarbeitungsgeschwindigkeit, Hemmung und Arbeitsgedächtnis. Bei entwicklungsbedingten Enzephalopathien ist die Beeinträchtigung umfassender, sodass interdisziplinäre Teams erforderlich sind.
Die Symptomatik epileptischer Patienten ähnelt oft anderen Neuroentwicklungsstörungen. Daher können Rehabilitationsstrategien aus anderen klinischen Bereichen (kognitive Stimulation, Optimierung oder Kompensation) angewendet werden.
Wichtigster Aspekt in der Intervention ist die Semiotik des Anfalls und seine Entwicklung, da sie kognitives Profil und Verlauf bestimmen.
Epilepsie in anderen Pathologien
Epilepsie tritt auch bei zerebraler Kinderlähmung, genetischen Syndromen, Autismus etc. auf und verschlechtert dort klinische Manifestationen oder verursacht neuropsychologische Regressionen.
Jede wiederkehrende Anfallsform beeinträchtigt kognitive Funktionen, auch als benign geltende kindliche Anfälle. Zwar fehlen initial Symptome, langfristig zeigen sich subtile Defizite (Aufmerksamkeit, Arbeitsgedächtnis, Hemmung). Daher sind auch hier Diagnostik und Monitoring wichtig.
Anforderungen an ein neuropsychologisches Rehabilitationsprogramm bei Epilepsie
Ein neuropsychologisches Rehabilitationsprogramm sollte:
- Auf theoretische Bezugsmodelle zurückgreifen,
- eine interdisziplinäre Perspektive im Umfeld des Kindes (Therapie, Schule, Familie) annehmen,
- Prioritäten klar festlegen,
- Einsatz möglichst früh beginnen,
- ausreichend Therapiedauer (fallabhängig) garantieren,
- auf erhaltene Fähigkeiten aufbauen,
- Emotionale und motivationale Variablen berücksichtigen,
- starke Familienunterstützung einbinden.
Bedeutung der Neurorehabilitation bei Epilepsie
Neurorehabilitation ist nicht nur für kognitive Stimulation und Rehabilita-tion entscheidend, sondern auch, um das kognitive Profil und Anfallsmuster zu verfolgen.
Neuropsychologische Behandlung ermöglicht ein fortlaufendes klinisches Monitoring und schult den Neuropsychologen in der Semiotik einzelner Patienten. So lassen sich subtile klinische Veränderungen oder neue Muster in Anfallsverläufen erkennen, verursacht durch medikamentöse Anpassungen, emotionale Zustände oder Überstimulierung.
Dies erlaubt, kognitive Verschlechterungen oder Krankheitsprogression zu dokumentieren und medikamentöse Anpassungen zu empfehlen, um Nebenwirkungen zu minimieren.
Abschließend sei betont, dass alle Programme (digital oder Papier) lediglich Werkzeuge zur Förderung betroffener Prozesse sind. Erfolg hängt vom definierten Ziel und der Methodik ab.
Kognitive Prozesse sind nicht unabhängig, insbesondere bei netzwerkbasierten Störungen wie Epilepsie. Das menschliche kognitive System beruht auf der Interaktion verschiedener neuropsychologischer Prozesse, die sich in Entwicklung und Erholung gegenseitig beeinflussen. Daher ist es wichtig, keine isolierte Funktionsrehabilitation anzustreben.
Wenn Ihnen dieser Artikel zu Klinischer Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie gefallen hat, könnten Sie auch an folgenden Beiträgen interessiert sein:
Dieser Artikel wurde übersetzt; Link zum Originalartikel auf Spanisch:
Neuropsicología clínica en la neurocirugía de la epilepsia pediátrica
- den Patienten longitudinal zu evaluieren,
- Vertrauen zum Kind und der Familie aufzubauen,
- Testtrainings für das intraoperative Mapping durchzuführen.
In dieser Zeit empfiehlt sich ein Programm zur neuropsychologischen Rehabilitation und Stimulation, um bessere prächirurgische, intraoperative Abläufe und eine Reduktion ängstlicher Krisen und posttraumatischer Belastungsreaktionen zu erreichen.
Kognitive Neurorehabilitation bei Epilepsie
Patientenfaktoren für Neurorehabilitationsprogramme
Das neuropsychologische Profil epileptischer Patienten variiert. Für Neurorehabilitation sind folgende Faktoren entscheidend:
1. Alter beim Anfallsbeginn
Das strukturelle und funktionelle Reifealter des Gehirns bestimmt klinische und neurophysiologische Ausdrucksformen. Früher Beginn erhöht Risiko kognitiver Beeinträchtigungen. Studien zeigen, dass das Alter 0–5 Jahre am kritischsten ist (Mauri et al., 2001).
2. Anfallstypen
Generalisierte Anfälle führen normalerweise zu stärkeren kognitiven Beeinträchtigungen als fokale Anfälle.
- Generalisierte Anfälle betreffen tiefe subcorticale Strukturen, Thalamus und retikuläres Formatio-System, die komplexe Funktionen steuern.
- Fokale Epilepsien sind oft mit spezifischen neuropsychologischen Defiziten je nach Anfallslokalisation verbunden (Mulas et al., 2006).
3. Anfallsfrequenz
Häufigere Anfälle beeinträchtigen kognitive Funktionen stärker.
4. Ätiologie oder Epilepsiesyndrom
Epileptische Enzephalopathien (z. B. West, Lennox-Gastaut) haben schlechteste Prognose mit progredienter Beeinträchtigung durch exzessive, diffuse elektrische Aktivität (Nieto, 2011).
5. Pharmakotherapie
Antiepileptika können durch Anfallskontrolle positive kognitive und emotionale Effekte haben, doch sie beeinflussen auch neuronale Netze, die Kognition regulieren, und können unerwünschte neuropsychologische Effekte verursachen.
Moderne Antiepileptika haben geringeren kognitiven Impact, doch zeigt sich in der Praxis weiter eine Beziehung zwischen Medikation und kognitiver Leistung. Beeinträchtigungen sind meist spezifisch und nicht generalisiert.
Monotherapie
Bei zu hohen Blutspiegeln oder rascher Dosissteigerung (Álvarez-Carriles et al., 2011) können auch zwei Medikamente mit geringem kognitiven Nebeneffekt kombinierte Probleme verursachen (Moog, 2009).
Die meisten Antiepileptika reduzieren Membranerregbarkeit, erhöhen postsynaptische Hemmung oder stören Netzsynchronisation. Dies verringert Verarbeitungs- und Aufmerksamkeitsgeschwindigkeit, was in sich entwickelnden Gehirnen stark einschränkend wirken kann.
Allgemeine Nebenwirkungen antiepileptischer Medikamente
Trotz individueller Unterschiede lassen sich folgende Nebenwirkungen festhalten:
- Aufmerksamkeits- und Hemmungsstörungen, verstärkt durch Sedierung oder Schlaflosigkeit,
- Verlangsamung der Informationsverarbeitung,
- Reizbarkeit,
- motorische Unruhe,
- emotionale Dysregulation,
- Beeinträchtigung des Arbeitsgedächtnisses,
- Visusveränderungen,
- usw. (Campos-Castelló & Campos-Soler, 2004).
Größere Defizite finden sich bei pharmakoresistenten Patienten, besonders mit frühem Erkrankungsbeginn, da sie langjährige Chronizität und mehrere Therapien erleben.
Dosis und Anstiegsraten müssen beachtet werden, da kognitive Symptome dosisabhängig zunehmen.
6. Hirnplastizität
Die funktionelle Reorganisation in pädiatrischer Epilepsie zeigt, dass Sprache und Gedächtnis flexibel sind und sich während der Entwicklung verlagern können – etwa von der linken Dominanzregion ins rechte Hemisphären-Pendant oder zu nichttraditionellen Regionen (Brazdil et al., 2005). Dennoch ist dies individuell sehr komplex und erfordert spezialisierte neuropsychologische Rehabilitation.
Diese Faktoren unterscheiden sich je Patient. In Epilepsie sind subkortikale Funktionen (Aufrechterhaltung der Aufmerksamkeit, Arbeitsgedächtnis, Verarbeitungsgeschwindigkeit, kategoriales Abrufen) primär betroffen und verschlechtern sich durch Medikamente zusätzlich.
Klinische und neuropsychologische Manifestationen bei Epilepsie
Primär betroffen sind Aufmerksamkeit, Gedächtnis, Sprache, Verarbeitungsgeschwindigkeit, Hemmung und Arbeitsgedächtnis. Bei entwicklungsbedingten Enzephalopathien ist die Beeinträchtigung umfassender, sodass interdisziplinäre Teams erforderlich sind.
Die Symptomatik epileptischer Patienten ähnelt oft anderen Neuroentwicklungsstörungen. Daher können Rehabilitationsstrategien aus anderen klinischen Bereichen (kognitive Stimulation, Optimierung oder Kompensation) angewendet werden.
Wichtigster Aspekt in der Intervention ist die Semiotik des Anfalls und seine Entwicklung, da sie kognitives Profil und Verlauf bestimmen.
Epilepsie in anderen Pathologien
Epilepsie tritt auch bei zerebraler Kinderlähmung, genetischen Syndromen, Autismus etc. auf und verschlechtert dort klinische Manifestationen oder verursacht neuropsychologische Regressionen.
Jede wiederkehrende Anfallsform beeinträchtigt kognitive Funktionen, auch als benign geltende kindliche Anfälle. Zwar fehlen initial Symptome, langfristig zeigen sich subtile Defizite (Aufmerksamkeit, Arbeitsgedächtnis, Hemmung). Daher sind auch hier Diagnostik und Monitoring wichtig.
Anforderungen an ein neuropsychologisches Rehabilitationsprogramm bei Epilepsie
Ein neuropsychologisches Rehabilitationsprogramm sollte:
- Auf theoretische Bezugsmodelle zurückgreifen,
- eine interdisziplinäre Perspektive im Umfeld des Kindes (Therapie, Schule, Familie) annehmen,
- Prioritäten klar festlegen,
- Einsatz möglichst früh beginnen,
- ausreichend Therapiedauer (fallabhängig) garantieren,
- auf erhaltene Fähigkeiten aufbauen,
- Emotionale und motivationale Variablen berücksichtigen,
- starke Familienunterstützung einbinden.
Bedeutung der Neurorehabilitation bei Epilepsie
Neurorehabilitation ist nicht nur für kognitive Stimulation und Rehabilita-tion entscheidend, sondern auch, um das kognitive Profil und Anfallsmuster zu verfolgen.
Neuropsychologische Behandlung ermöglicht ein fortlaufendes klinisches Monitoring und schult den Neuropsychologen in der Semiotik einzelner Patienten. So lassen sich subtile klinische Veränderungen oder neue Muster in Anfallsverläufen erkennen, verursacht durch medikamentöse Anpassungen, emotionale Zustände oder Überstimulierung.
Dies erlaubt, kognitive Verschlechterungen oder Krankheitsprogression zu dokumentieren und medikamentöse Anpassungen zu empfehlen, um Nebenwirkungen zu minimieren.
Abschließend sei betont, dass alle Programme (digital oder Papier) lediglich Werkzeuge zur Förderung betroffener Prozesse sind. Erfolg hängt vom definierten Ziel und der Methodik ab.
Kognitive Prozesse sind nicht unabhängig, insbesondere bei netzwerkbasierten Störungen wie Epilepsie. Das menschliche kognitive System beruht auf der Interaktion verschiedener neuropsychologischer Prozesse, die sich in Entwicklung und Erholung gegenseitig beeinflussen. Daher ist es wichtig, keine isolierte Funktionsrehabilitation anzustreben.
Wenn Ihnen dieser Artikel zu Klinischer Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie gefallen hat, könnten Sie auch an folgenden Beiträgen interessiert sein:
Dieser Artikel wurde übersetzt; Link zum Originalartikel auf Spanisch:
Neuropsicología clínica en la neurocirugía de la epilepsia pediátrica
- Ätiologie der Läsion,
- Alter bei Anfallsbeginn,
- Alter zur OP,
- Interventionsart und Komplikationen,
- medikamentöse Therapie,
- interventionelles Umfeld,
- Zugang zu vorangegangener Neurorehabilitation,
- usw.
Bessere Anfallskontrolle oder Reduktion antiepileptischer Medikamente führt zu deutlicher neurokognitiver Verbesserung.
Die verfügbare Evidenz stammt meist aus Einzelfällen oder kurzen Fallserien. Es bedarf weiterer Dokumentation der neuropsychologischen Entwicklung zur besseren Abwägung von Risiken und Nutzen früher radikaler Eingriffe (Fournier, 2019).
Spezifische Protokolle ähneln den oben genannten, mit Vertiefung in Sprache, Gedächtnis oder visuell-räumliche Funktionen oder Ergänzung psychopatologischer Skalen.
Nachsorge
In der chirurgischen Nachsorge ist es wichtig, das Bewusstsein und grundlegende Funktionen des Kindes beim Aufwachen, in den folgenden Tagen und sechs Monate postoperativ umfassend neuropsychologisch zu bewerten. Ziel ist, Rehabilitations- und Bildungsprogramme festzulegen.
In einigen Fällen (meist 7–8 Jahre) und je nach Läsionslage in eloquenter Zone kann ein intraoperatives Mapping mit wachem Patienten erwogen werden. Hier muss der Neuropsychologe den Patienten im Vorfeld an Tests und Abläufe gewöhnen.
Meist versucht man jedoch, wache intraoperative Protokolle bei Kindern zu vermeiden und greift auf funktionelle MRT oder Wada-Test zurück.
Wenn keine klaren Daten vorliegen oder das Risiko in eloquenter Zone (Sprache, Gedächtnis) hoch ist, ist ein intraoperatives Hirnmapping notwendig. Wann möglich, sollte Monate vor der OP ein longitudinales neuropsychologisches Protokoll erfolgen, um:
- den Patienten longitudinal zu evaluieren,
- Vertrauen zum Kind und der Familie aufzubauen,
- Testtrainings für das intraoperative Mapping durchzuführen.
In dieser Zeit empfiehlt sich ein Programm zur neuropsychologischen Rehabilitation und Stimulation, um bessere prächirurgische, intraoperative Abläufe und eine Reduktion ängstlicher Krisen und posttraumatischer Belastungsreaktionen zu erreichen.
Kognitive Neurorehabilitation bei Epilepsie
Patientenfaktoren für Neurorehabilitationsprogramme
Das neuropsychologische Profil epileptischer Patienten variiert. Für Neurorehabilitation sind folgende Faktoren entscheidend:
1. Alter beim Anfallsbeginn
Das strukturelle und funktionelle Reifealter des Gehirns bestimmt klinische und neurophysiologische Ausdrucksformen. Früher Beginn erhöht Risiko kognitiver Beeinträchtigungen. Studien zeigen, dass das Alter 0–5 Jahre am kritischsten ist (Mauri et al., 2001).
2. Anfallstypen
Generalisierte Anfälle führen normalerweise zu stärkeren kognitiven Beeinträchtigungen als fokale Anfälle.
- Generalisierte Anfälle betreffen tiefe subcorticale Strukturen, Thalamus und retikuläres Formatio-System, die komplexe Funktionen steuern.
- Fokale Epilepsien sind oft mit spezifischen neuropsychologischen Defiziten je nach Anfallslokalisation verbunden (Mulas et al., 2006).
3. Anfallsfrequenz
Häufigere Anfälle beeinträchtigen kognitive Funktionen stärker.
4. Ätiologie oder Epilepsiesyndrom
Epileptische Enzephalopathien (z. B. West, Lennox-Gastaut) haben schlechteste Prognose mit progredienter Beeinträchtigung durch exzessive, diffuse elektrische Aktivität (Nieto, 2011).
5. Pharmakotherapie
Antiepileptika können durch Anfallskontrolle positive kognitive und emotionale Effekte haben, doch sie beeinflussen auch neuronale Netze, die Kognition regulieren, und können unerwünschte neuropsychologische Effekte verursachen.
Moderne Antiepileptika haben geringeren kognitiven Impact, doch zeigt sich in der Praxis weiter eine Beziehung zwischen Medikation und kognitiver Leistung. Beeinträchtigungen sind meist spezifisch und nicht generalisiert.
Monotherapie
Bei zu hohen Blutspiegeln oder rascher Dosissteigerung (Álvarez-Carriles et al., 2011) können auch zwei Medikamente mit geringem kognitiven Nebeneffekt kombinierte Probleme verursachen (Moog, 2009).
Die meisten Antiepileptika reduzieren Membranerregbarkeit, erhöhen postsynaptische Hemmung oder stören Netzsynchronisation. Dies verringert Verarbeitungs- und Aufmerksamkeitsgeschwindigkeit, was in sich entwickelnden Gehirnen stark einschränkend wirken kann.
Allgemeine Nebenwirkungen antiepileptischer Medikamente
Trotz individueller Unterschiede lassen sich folgende Nebenwirkungen festhalten:
- Aufmerksamkeits- und Hemmungsstörungen, verstärkt durch Sedierung oder Schlaflosigkeit,
- Verlangsamung der Informationsverarbeitung,
- Reizbarkeit,
- motorische Unruhe,
- emotionale Dysregulation,
- Beeinträchtigung des Arbeitsgedächtnisses,
- Visusveränderungen,
- usw. (Campos-Castelló & Campos-Soler, 2004).
Größere Defizite finden sich bei pharmakoresistenten Patienten, besonders mit frühem Erkrankungsbeginn, da sie langjährige Chronizität und mehrere Therapien erleben.
Dosis und Anstiegsraten müssen beachtet werden, da kognitive Symptome dosisabhängig zunehmen.
6. Hirnplastizität
Die funktionelle Reorganisation in pädiatrischer Epilepsie zeigt, dass Sprache und Gedächtnis flexibel sind und sich während der Entwicklung verlagern können – etwa von der linken Dominanzregion ins rechte Hemisphären-Pendant oder zu nichttraditionellen Regionen (Brazdil et al., 2005). Dennoch ist dies individuell sehr komplex und erfordert spezialisierte neuropsychologische Rehabilitation.
Diese Faktoren unterscheiden sich je Patient. In Epilepsie sind subkortikale Funktionen (Aufrechterhaltung der Aufmerksamkeit, Arbeitsgedächtnis, Verarbeitungsgeschwindigkeit, kategoriales Abrufen) primär betroffen und verschlechtern sich durch Medikamente zusätzlich.
Klinische und neuropsychologische Manifestationen bei Epilepsie
Primär betroffen sind Aufmerksamkeit, Gedächtnis, Sprache, Verarbeitungsgeschwindigkeit, Hemmung und Arbeitsgedächtnis. Bei entwicklungsbedingten Enzephalopathien ist die Beeinträchtigung umfassender, sodass interdisziplinäre Teams erforderlich sind.
Die Symptomatik epileptischer Patienten ähnelt oft anderen Neuroentwicklungsstörungen. Daher können Rehabilitationsstrategien aus anderen klinischen Bereichen (kognitive Stimulation, Optimierung oder Kompensation) angewendet werden.
Wichtigster Aspekt in der Intervention ist die Semiotik des Anfalls und seine Entwicklung, da sie kognitives Profil und Verlauf bestimmen.
Epilepsie in anderen Pathologien
Epilepsie tritt auch bei zerebraler Kinderlähmung, genetischen Syndromen, Autismus etc. auf und verschlechtert dort klinische Manifestationen oder verursacht neuropsychologische Regressionen.
Jede wiederkehrende Anfallsform beeinträchtigt kognitive Funktionen, auch als benign geltende kindliche Anfälle. Zwar fehlen initial Symptome, langfristig zeigen sich subtile Defizite (Aufmerksamkeit, Arbeitsgedächtnis, Hemmung). Daher sind auch hier Diagnostik und Monitoring wichtig.
Anforderungen an ein neuropsychologisches Rehabilitationsprogramm bei Epilepsie
Ein neuropsychologisches Rehabilitationsprogramm sollte:
- Auf theoretische Bezugsmodelle zurückgreifen,
- eine interdisziplinäre Perspektive im Umfeld des Kindes (Therapie, Schule, Familie) annehmen,
- Prioritäten klar festlegen,
- Einsatz möglichst früh beginnen,
- ausreichend Therapiedauer (fallabhängig) garantieren,
- auf erhaltene Fähigkeiten aufbauen,
- Emotionale und motivationale Variablen berücksichtigen,
- starke Familienunterstützung einbinden.
Bedeutung der Neurorehabilitation bei Epilepsie
Neurorehabilitation ist nicht nur für kognitive Stimulation und Rehabilita-tion entscheidend, sondern auch, um das kognitive Profil und Anfallsmuster zu verfolgen.
Neuropsychologische Behandlung ermöglicht ein fortlaufendes klinisches Monitoring und schult den Neuropsychologen in der Semiotik einzelner Patienten. So lassen sich subtile klinische Veränderungen oder neue Muster in Anfallsverläufen erkennen, verursacht durch medikamentöse Anpassungen, emotionale Zustände oder Überstimulierung.
Dies erlaubt, kognitive Verschlechterungen oder Krankheitsprogression zu dokumentieren und medikamentöse Anpassungen zu empfehlen, um Nebenwirkungen zu minimieren.
Abschließend sei betont, dass alle Programme (digital oder Papier) lediglich Werkzeuge zur Förderung betroffener Prozesse sind. Erfolg hängt vom definierten Ziel und der Methodik ab.
Kognitive Prozesse sind nicht unabhängig, insbesondere bei netzwerkbasierten Störungen wie Epilepsie. Das menschliche kognitive System beruht auf der Interaktion verschiedener neuropsychologischer Prozesse, die sich in Entwicklung und Erholung gegenseitig beeinflussen. Daher ist es wichtig, keine isolierte Funktionsrehabilitation anzustreben.
Wenn Ihnen dieser Artikel zu Klinischer Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie gefallen hat, könnten Sie auch an folgenden Beiträgen interessiert sein:
Dieser Artikel wurde übersetzt; Link zum Originalartikel auf Spanisch:
Neuropsicología clínica en la neurocirugía de la epilepsia pediátrica
Im pädiatrischen Bereich ist die Rolle des Neuropsychologen noch wichtiger, da er Vertrauen zum Kind aufbaut und die Familie unterstützt.
Hirnplastizität
Die Plastizität im Kindesalter ist entscheidend für die Operationsplanung, nicht nur wegen kognitiver Reorganisation, sondern auch wegen der chronischen Anfallsfolgen in der Neuroentwicklung.
Der neurokognitive Verlauf nach Operation hängt von vielen Faktoren ab:
- Ätiologie der Läsion,
- Alter bei Anfallsbeginn,
- Alter zur OP,
- Interventionsart und Komplikationen,
- medikamentöse Therapie,
- interventionelles Umfeld,
- Zugang zu vorangegangener Neurorehabilitation,
- usw.
Bessere Anfallskontrolle oder Reduktion antiepileptischer Medikamente führt zu deutlicher neurokognitiver Verbesserung.
Die verfügbare Evidenz stammt meist aus Einzelfällen oder kurzen Fallserien. Es bedarf weiterer Dokumentation der neuropsychologischen Entwicklung zur besseren Abwägung von Risiken und Nutzen früher radikaler Eingriffe (Fournier, 2019).
Spezifische Protokolle ähneln den oben genannten, mit Vertiefung in Sprache, Gedächtnis oder visuell-räumliche Funktionen oder Ergänzung psychopatologischer Skalen.
Nachsorge
In der chirurgischen Nachsorge ist es wichtig, das Bewusstsein und grundlegende Funktionen des Kindes beim Aufwachen, in den folgenden Tagen und sechs Monate postoperativ umfassend neuropsychologisch zu bewerten. Ziel ist, Rehabilitations- und Bildungsprogramme festzulegen.
In einigen Fällen (meist 7–8 Jahre) und je nach Läsionslage in eloquenter Zone kann ein intraoperatives Mapping mit wachem Patienten erwogen werden. Hier muss der Neuropsychologe den Patienten im Vorfeld an Tests und Abläufe gewöhnen.
Meist versucht man jedoch, wache intraoperative Protokolle bei Kindern zu vermeiden und greift auf funktionelle MRT oder Wada-Test zurück.
Wenn keine klaren Daten vorliegen oder das Risiko in eloquenter Zone (Sprache, Gedächtnis) hoch ist, ist ein intraoperatives Hirnmapping notwendig. Wann möglich, sollte Monate vor der OP ein longitudinales neuropsychologisches Protokoll erfolgen, um:
- den Patienten longitudinal zu evaluieren,
- Vertrauen zum Kind und der Familie aufzubauen,
- Testtrainings für das intraoperative Mapping durchzuführen.
In dieser Zeit empfiehlt sich ein Programm zur neuropsychologischen Rehabilitation und Stimulation, um bessere prächirurgische, intraoperative Abläufe und eine Reduktion ängstlicher Krisen und posttraumatischer Belastungsreaktionen zu erreichen.
Kognitive Neurorehabilitation bei Epilepsie
Patientenfaktoren für Neurorehabilitationsprogramme
Das neuropsychologische Profil epileptischer Patienten variiert. Für Neurorehabilitation sind folgende Faktoren entscheidend:
1. Alter beim Anfallsbeginn
Das strukturelle und funktionelle Reifealter des Gehirns bestimmt klinische und neurophysiologische Ausdrucksformen. Früher Beginn erhöht Risiko kognitiver Beeinträchtigungen. Studien zeigen, dass das Alter 0–5 Jahre am kritischsten ist (Mauri et al., 2001).
2. Anfallstypen
Generalisierte Anfälle führen normalerweise zu stärkeren kognitiven Beeinträchtigungen als fokale Anfälle.
- Generalisierte Anfälle betreffen tiefe subcorticale Strukturen, Thalamus und retikuläres Formatio-System, die komplexe Funktionen steuern.
- Fokale Epilepsien sind oft mit spezifischen neuropsychologischen Defiziten je nach Anfallslokalisation verbunden (Mulas et al., 2006).
3. Anfallsfrequenz
Häufigere Anfälle beeinträchtigen kognitive Funktionen stärker.
4. Ätiologie oder Epilepsiesyndrom
Epileptische Enzephalopathien (z. B. West, Lennox-Gastaut) haben schlechteste Prognose mit progredienter Beeinträchtigung durch exzessive, diffuse elektrische Aktivität (Nieto, 2011).
5. Pharmakotherapie
Antiepileptika können durch Anfallskontrolle positive kognitive und emotionale Effekte haben, doch sie beeinflussen auch neuronale Netze, die Kognition regulieren, und können unerwünschte neuropsychologische Effekte verursachen.
Moderne Antiepileptika haben geringeren kognitiven Impact, doch zeigt sich in der Praxis weiter eine Beziehung zwischen Medikation und kognitiver Leistung. Beeinträchtigungen sind meist spezifisch und nicht generalisiert.
Monotherapie
Bei zu hohen Blutspiegeln oder rascher Dosissteigerung (Álvarez-Carriles et al., 2011) können auch zwei Medikamente mit geringem kognitiven Nebeneffekt kombinierte Probleme verursachen (Moog, 2009).
Die meisten Antiepileptika reduzieren Membranerregbarkeit, erhöhen postsynaptische Hemmung oder stören Netzsynchronisation. Dies verringert Verarbeitungs- und Aufmerksamkeitsgeschwindigkeit, was in sich entwickelnden Gehirnen stark einschränkend wirken kann.
Allgemeine Nebenwirkungen antiepileptischer Medikamente
Trotz individueller Unterschiede lassen sich folgende Nebenwirkungen festhalten:
- Aufmerksamkeits- und Hemmungsstörungen, verstärkt durch Sedierung oder Schlaflosigkeit,
- Verlangsamung der Informationsverarbeitung,
- Reizbarkeit,
- motorische Unruhe,
- emotionale Dysregulation,
- Beeinträchtigung des Arbeitsgedächtnisses,
- Visusveränderungen,
- usw. (Campos-Castelló & Campos-Soler, 2004).
Größere Defizite finden sich bei pharmakoresistenten Patienten, besonders mit frühem Erkrankungsbeginn, da sie langjährige Chronizität und mehrere Therapien erleben.
Dosis und Anstiegsraten müssen beachtet werden, da kognitive Symptome dosisabhängig zunehmen.
6. Hirnplastizität
Die funktionelle Reorganisation in pädiatrischer Epilepsie zeigt, dass Sprache und Gedächtnis flexibel sind und sich während der Entwicklung verlagern können – etwa von der linken Dominanzregion ins rechte Hemisphären-Pendant oder zu nichttraditionellen Regionen (Brazdil et al., 2005). Dennoch ist dies individuell sehr komplex und erfordert spezialisierte neuropsychologische Rehabilitation.
Diese Faktoren unterscheiden sich je Patient. In Epilepsie sind subkortikale Funktionen (Aufrechterhaltung der Aufmerksamkeit, Arbeitsgedächtnis, Verarbeitungsgeschwindigkeit, kategoriales Abrufen) primär betroffen und verschlechtern sich durch Medikamente zusätzlich.
Klinische und neuropsychologische Manifestationen bei Epilepsie
Primär betroffen sind Aufmerksamkeit, Gedächtnis, Sprache, Verarbeitungsgeschwindigkeit, Hemmung und Arbeitsgedächtnis. Bei entwicklungsbedingten Enzephalopathien ist die Beeinträchtigung umfassender, sodass interdisziplinäre Teams erforderlich sind.
Die Symptomatik epileptischer Patienten ähnelt oft anderen Neuroentwicklungsstörungen. Daher können Rehabilitationsstrategien aus anderen klinischen Bereichen (kognitive Stimulation, Optimierung oder Kompensation) angewendet werden.
Wichtigster Aspekt in der Intervention ist die Semiotik des Anfalls und seine Entwicklung, da sie kognitives Profil und Verlauf bestimmen.
Epilepsie in anderen Pathologien
Epilepsie tritt auch bei zerebraler Kinderlähmung, genetischen Syndromen, Autismus etc. auf und verschlechtert dort klinische Manifestationen oder verursacht neuropsychologische Regressionen.
Jede wiederkehrende Anfallsform beeinträchtigt kognitive Funktionen, auch als benign geltende kindliche Anfälle. Zwar fehlen initial Symptome, langfristig zeigen sich subtile Defizite (Aufmerksamkeit, Arbeitsgedächtnis, Hemmung). Daher sind auch hier Diagnostik und Monitoring wichtig.
Anforderungen an ein neuropsychologisches Rehabilitationsprogramm bei Epilepsie
Ein neuropsychologisches Rehabilitationsprogramm sollte:
- Auf theoretische Bezugsmodelle zurückgreifen,
- eine interdisziplinäre Perspektive im Umfeld des Kindes (Therapie, Schule, Familie) annehmen,
- Prioritäten klar festlegen,
- Einsatz möglichst früh beginnen,
- ausreichend Therapiedauer (fallabhängig) garantieren,
- auf erhaltene Fähigkeiten aufbauen,
- Emotionale und motivationale Variablen berücksichtigen,
- starke Familienunterstützung einbinden.
Bedeutung der Neurorehabilitation bei Epilepsie
Neurorehabilitation ist nicht nur für kognitive Stimulation und Rehabilita-tion entscheidend, sondern auch, um das kognitive Profil und Anfallsmuster zu verfolgen.
Neuropsychologische Behandlung ermöglicht ein fortlaufendes klinisches Monitoring und schult den Neuropsychologen in der Semiotik einzelner Patienten. So lassen sich subtile klinische Veränderungen oder neue Muster in Anfallsverläufen erkennen, verursacht durch medikamentöse Anpassungen, emotionale Zustände oder Überstimulierung.
Dies erlaubt, kognitive Verschlechterungen oder Krankheitsprogression zu dokumentieren und medikamentöse Anpassungen zu empfehlen, um Nebenwirkungen zu minimieren.
Abschließend sei betont, dass alle Programme (digital oder Papier) lediglich Werkzeuge zur Förderung betroffener Prozesse sind. Erfolg hängt vom definierten Ziel und der Methodik ab.
Kognitive Prozesse sind nicht unabhängig, insbesondere bei netzwerkbasierten Störungen wie Epilepsie. Das menschliche kognitive System beruht auf der Interaktion verschiedener neuropsychologischer Prozesse, die sich in Entwicklung und Erholung gegenseitig beeinflussen. Daher ist es wichtig, keine isolierte Funktionsrehabilitation anzustreben.
Wenn Ihnen dieser Artikel zu Klinischer Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie gefallen hat, könnten Sie auch an folgenden Beiträgen interessiert sein:
Dieser Artikel wurde übersetzt; Link zum Originalartikel auf Spanisch:
Neuropsicología clínica en la neurocirugía de la epilepsia pediátrica
- Familiäre benign infantile Anfälle (klingen bis zum 2. Lebensjahr ab, ohne Langzeitfolgen),
- Epileptische Enzephalopathie im Säuglingsalter (schwer kontrollierbare Anfälle <1 Jahr, gefolgt von Entwicklungsverzögerung),
- Autismus-Spektrum-Störung, wobei ca. 30 % später Epilepsie entwickeln (nach dem 12. Monat).
Diese genetisch bedingten Epilepsien führten dazu, dass die ILAE 2017 den Begriff „epileptische Enzephalopathie“ auf „Entwicklungs- und epileptische Enzephalopathie“ erweiterte, um Epilepsie uneingeschränkt als Entwicklungsstörung anzuerkennen.
Dies ist ein weiterer Fortschritt in Richtung Anerkennung kindlicher Epilepsie als Neuroentwicklungsstörung, unterstützt von immer mehr Forschungsergebnissen.
Neuropsychologische Diagnostik und Rolle des klinischen Neuropsychologen bei pädiatrischer Epilepsie
Heute gewinnt nicht nur die neuropsychologische Diagnostik von Epilepsiepatienten zunehmend an Bedeutung, sondern auch die Rolle des Neuropsychologen in Epilepsieteams für Diagnostik, chirurgische Intervention und Rehabilitation.
Bei Kindern liefert die neuropsychologische Untersuchung wesentliche Informationen zur Betreuung und Anleitung. Epilepsie kann im sich entwickelnden Gehirn Dysfunktionen in weitreichenden Netzwerken festigen (Fournier, 2019).
Die Ziele der Diagnostik sind diagnostischer Natur: Kognitive oder Verhaltensstörungen liefern wichtige Hinweise zur Lokalisation und Lateralisation der Anfälle, was für die Epilepsiechirurgie sehr hilfreich ist. Zudem unterstützt sie ein besseres Verständnis des Epilepsiesyndroms und damit fundiertere therapeutische Entscheidungen, pharmacologisch und non-pharmacologisch.
Ziele einer neuropsychologischen Untersuchung bei pädiatrischer Epilepsie
Nach Chulune (2010) lassen sich folgende Ziele hervorheben:
- Erfassung eines neuropsychologischen Basisprofils, um Risiken für Entwicklungs-, kognitive, schulische oder psychopathologische Probleme ab dem ersten Anfall zu erkennen.
- Erleichterung der Erkennung neurologischer Störungen, die bei Kindern oft unbemerkt bleiben und als normale Entwicklungsverzögerung fehlgedeutet werden.
- Monitoring kognitiver und Verhaltensänderungen im Krankheitsverlauf.
- Diagnose psychopathologischer Auffälligkeiten und Bewertung ihrer Auswirkung auf Kognition und adaptive Fähigkeiten.
- Unterstützung bei Therapie- und Förderungsplänen und schulischer Maßnahmen.
- Dokumentation möglicher unerwünschter Nebenwirkungen antiepileptischer Medikamente auf kognitiver und verhaltensbezogener Ebene.
Die ILAE empfiehlt, die neuropsychologische Diagnostik als Teil der Routineversorgung von Epilepsiepatienten zu integrieren (Wilson et al., 2015). Der klinische Neuropsychologe sollte weit über Testadministration und statistische Auswertung hinaus aktiv sein, mit umfassender Ausbildung und langjähriger Erfahrung in klinischer und entwicklungsbezogener Neuropsychologie.
Die Analyse der kognitiven Semiotik gewinnt an Bedeutung, um Informationen aus Testverfahren mit der Krankengeschichte und Untersuchung des Patienten zu synthetisieren.
Angesichts der Schwierigkeiten, strukturierte Protokolle bei jungen Kindern mit ausgeprägten Entwicklungsstörungen anzuwenden, ist Anpassungsfähigkeit des Neuropsychologen gefragt, um ein belastbares kognitives Profil zu erstellen.
Neuropsychologische Testprotokolle
Wegen der speziellen Epilepsiefolgen in der Kindheit sind Standardprotokolle, wie bei Erwachsenen, schwer anzuwenden. Internationale und nationale Leitlinien für Kinder existieren kaum.
Wichtig ist, dass man keine noch in Entwicklung befindlichen Funktionen testet. Faktoren wie Aufmerksamkeit, Müdigkeit oder emotionsbedingte Einflüsse sind bei Kindern stärker ausgeprägt. Daher empfiehlt sich Flexibilität, Einführung des Kindes beim Untersucher und Zeitneutralität.
Screening-Tests alleine reichen nicht aus; das Protokoll muss breit genug sein, um verschiedene kognitive Domänen abzudecken. Funktionen wie Gedächtnis sind unter 5 Jahren oft nicht zuverlässig zu prüfen.
Bei exekutiven Funktionen sind verfügbare Tests hoch sensitiv, aber weniger spezifisch, da Sedierung und verlangsamte Informationsverarbeitung durch Antiepileptika viele Ergebnisse sekundär beeinflussen. Somit gewinnen kognitive Semiotik und qualitative Analysen an Bedeutung.
Klinische Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie
Epilepsiechirurgie bei Kindern wird oft nicht als Hauptbehandlungsoption gesehen, sollte aber nicht nur als letzter Schritt bei pharmakoresistenten Fällen betrachtet werden.
Angesichts der Bedeutung des sich entwickelnden Gehirns ist das Hauptziel aller Epilepsiechirurgieteams, die neuroentwicklungsprognose nicht zu verschlechtern. Hierbei ist der Beitrag der Neuropsychologie entscheidend. Der Neuropsychologe ist aktiv bei Auswahl, Evaluation, intraoperativer Betreuung und vor allem postoperativer Anleitung von Familie und Reha-Teams.
Dank fortgeschrittener struktureller und funktioneller Bildgebung lassen sich Kandidaten mit refraktären Läsionen besser erkennen (Berg et al., 2017).
Hauptziele einer neuropsychologischen Untersuchung bei Epilepsiechirurgie
Nach ILAE-Protokoll (Jayakar et al., 2014) sind die Ziele:
- Erstellung einer Basislinie, um Operationsauswirkungen quantitativ zu erfassen,
- Charakterisierung kognitiver Stärken und Defizite, teils vorher unentdeckt,
- Unterstützung bei Lokalisation oder Lateralisation kognitiver Funktionen,
- Information über Risiken postoperativer Defizite,
- Planung von Bildungs- und Rehabilitationsmaßnahmen für Kinder.
Standardpräoperatives Protokoll
- Strukturelles Hochauflösungs-Bildgebungsstudium (3 Tesla MRT),
- Neurophysiologisches Studium mit Video-EEG-Monitoring,
- Komplette neuropsychologische Untersuchung.
Für bestmögliche postoperative Ergebnisse (vollständige Läsionsresektion bei minimalen Funktionseinschränkungen) ist eine exakte Lokalisierung der epileptogenen Zone unerlässlich.
Weshalb es wichtig ist, zwischen symptomatischer Zone (Kortexregion, die durch Entladung Iktalzeichen erzeugt) und irritativer Zone (Region, die interiktale Entladungen generiert und durch EEG/MRT lokalisiert wird) zu unterscheiden.
Entladungen allein erzeugen selten Symptome; meist sind post-entladungsstarke Wellen durch Propagation verantwortlich. Nur selten, wenn Anfälle in eloquenter Zone entstehen, zeigen sich Symptome (Rosenow & Lüders, 2001).
Eine vollständige Läsionsentfernung ist nicht immer nötig und trotz kompletter Resektion können Anfälle persistieren (López & Pomposo-Graztela, 2001). Studien liefern meist nur einen Überblick über Läsionen („Eisbergspitze“), sodass viele finale Resektionsentscheidungen intraoperativ mit direkter Läsionsinformation getroffen werden. Deshalb ist die Präsenz des Neuropsychologen im OP, auch ohne waches Aufwachen, notwendig.
Im pädiatrischen Bereich ist die Rolle des Neuropsychologen noch wichtiger, da er Vertrauen zum Kind aufbaut und die Familie unterstützt.
Hirnplastizität
Die Plastizität im Kindesalter ist entscheidend für die Operationsplanung, nicht nur wegen kognitiver Reorganisation, sondern auch wegen der chronischen Anfallsfolgen in der Neuroentwicklung.
Der neurokognitive Verlauf nach Operation hängt von vielen Faktoren ab:
- Ätiologie der Läsion,
- Alter bei Anfallsbeginn,
- Alter zur OP,
- Interventionsart und Komplikationen,
- medikamentöse Therapie,
- interventionelles Umfeld,
- Zugang zu vorangegangener Neurorehabilitation,
- usw.
Bessere Anfallskontrolle oder Reduktion antiepileptischer Medikamente führt zu deutlicher neurokognitiver Verbesserung.
Die verfügbare Evidenz stammt meist aus Einzelfällen oder kurzen Fallserien. Es bedarf weiterer Dokumentation der neuropsychologischen Entwicklung zur besseren Abwägung von Risiken und Nutzen früher radikaler Eingriffe (Fournier, 2019).
Spezifische Protokolle ähneln den oben genannten, mit Vertiefung in Sprache, Gedächtnis oder visuell-räumliche Funktionen oder Ergänzung psychopatologischer Skalen.
Nachsorge
In der chirurgischen Nachsorge ist es wichtig, das Bewusstsein und grundlegende Funktionen des Kindes beim Aufwachen, in den folgenden Tagen und sechs Monate postoperativ umfassend neuropsychologisch zu bewerten. Ziel ist, Rehabilitations- und Bildungsprogramme festzulegen.
In einigen Fällen (meist 7–8 Jahre) und je nach Läsionslage in eloquenter Zone kann ein intraoperatives Mapping mit wachem Patienten erwogen werden. Hier muss der Neuropsychologe den Patienten im Vorfeld an Tests und Abläufe gewöhnen.
Meist versucht man jedoch, wache intraoperative Protokolle bei Kindern zu vermeiden und greift auf funktionelle MRT oder Wada-Test zurück.
Wenn keine klaren Daten vorliegen oder das Risiko in eloquenter Zone (Sprache, Gedächtnis) hoch ist, ist ein intraoperatives Hirnmapping notwendig. Wann möglich, sollte Monate vor der OP ein longitudinales neuropsychologisches Protokoll erfolgen, um:
- den Patienten longitudinal zu evaluieren,
- Vertrauen zum Kind und der Familie aufzubauen,
- Testtrainings für das intraoperative Mapping durchzuführen.
In dieser Zeit empfiehlt sich ein Programm zur neuropsychologischen Rehabilitation und Stimulation, um bessere prächirurgische, intraoperative Abläufe und eine Reduktion ängstlicher Krisen und posttraumatischer Belastungsreaktionen zu erreichen.
Kognitive Neurorehabilitation bei Epilepsie
Patientenfaktoren für Neurorehabilitationsprogramme
Das neuropsychologische Profil epileptischer Patienten variiert. Für Neurorehabilitation sind folgende Faktoren entscheidend:
1. Alter beim Anfallsbeginn
Das strukturelle und funktionelle Reifealter des Gehirns bestimmt klinische und neurophysiologische Ausdrucksformen. Früher Beginn erhöht Risiko kognitiver Beeinträchtigungen. Studien zeigen, dass das Alter 0–5 Jahre am kritischsten ist (Mauri et al., 2001).
2. Anfallstypen
Generalisierte Anfälle führen normalerweise zu stärkeren kognitiven Beeinträchtigungen als fokale Anfälle.
- Generalisierte Anfälle betreffen tiefe subcorticale Strukturen, Thalamus und retikuläres Formatio-System, die komplexe Funktionen steuern.
- Fokale Epilepsien sind oft mit spezifischen neuropsychologischen Defiziten je nach Anfallslokalisation verbunden (Mulas et al., 2006).
3. Anfallsfrequenz
Häufigere Anfälle beeinträchtigen kognitive Funktionen stärker.
4. Ätiologie oder Epilepsiesyndrom
Epileptische Enzephalopathien (z. B. West, Lennox-Gastaut) haben schlechteste Prognose mit progredienter Beeinträchtigung durch exzessive, diffuse elektrische Aktivität (Nieto, 2011).
5. Pharmakotherapie
Antiepileptika können durch Anfallskontrolle positive kognitive und emotionale Effekte haben, doch sie beeinflussen auch neuronale Netze, die Kognition regulieren, und können unerwünschte neuropsychologische Effekte verursachen.
Moderne Antiepileptika haben geringeren kognitiven Impact, doch zeigt sich in der Praxis weiter eine Beziehung zwischen Medikation und kognitiver Leistung. Beeinträchtigungen sind meist spezifisch und nicht generalisiert.
Monotherapie
Bei zu hohen Blutspiegeln oder rascher Dosissteigerung (Álvarez-Carriles et al., 2011) können auch zwei Medikamente mit geringem kognitiven Nebeneffekt kombinierte Probleme verursachen (Moog, 2009).
Die meisten Antiepileptika reduzieren Membranerregbarkeit, erhöhen postsynaptische Hemmung oder stören Netzsynchronisation. Dies verringert Verarbeitungs- und Aufmerksamkeitsgeschwindigkeit, was in sich entwickelnden Gehirnen stark einschränkend wirken kann.
Allgemeine Nebenwirkungen antiepileptischer Medikamente
Trotz individueller Unterschiede lassen sich folgende Nebenwirkungen festhalten:
- Aufmerksamkeits- und Hemmungsstörungen, verstärkt durch Sedierung oder Schlaflosigkeit,
- Verlangsamung der Informationsverarbeitung,
- Reizbarkeit,
- motorische Unruhe,
- emotionale Dysregulation,
- Beeinträchtigung des Arbeitsgedächtnisses,
- Visusveränderungen,
- usw. (Campos-Castelló & Campos-Soler, 2004).
Größere Defizite finden sich bei pharmakoresistenten Patienten, besonders mit frühem Erkrankungsbeginn, da sie langjährige Chronizität und mehrere Therapien erleben.
Dosis und Anstiegsraten müssen beachtet werden, da kognitive Symptome dosisabhängig zunehmen.
6. Hirnplastizität
Die funktionelle Reorganisation in pädiatrischer Epilepsie zeigt, dass Sprache und Gedächtnis flexibel sind und sich während der Entwicklung verlagern können – etwa von der linken Dominanzregion ins rechte Hemisphären-Pendant oder zu nichttraditionellen Regionen (Brazdil et al., 2005). Dennoch ist dies individuell sehr komplex und erfordert spezialisierte neuropsychologische Rehabilitation.
Diese Faktoren unterscheiden sich je Patient. In Epilepsie sind subkortikale Funktionen (Aufrechterhaltung der Aufmerksamkeit, Arbeitsgedächtnis, Verarbeitungsgeschwindigkeit, kategoriales Abrufen) primär betroffen und verschlechtern sich durch Medikamente zusätzlich.
Klinische und neuropsychologische Manifestationen bei Epilepsie
Primär betroffen sind Aufmerksamkeit, Gedächtnis, Sprache, Verarbeitungsgeschwindigkeit, Hemmung und Arbeitsgedächtnis. Bei entwicklungsbedingten Enzephalopathien ist die Beeinträchtigung umfassender, sodass interdisziplinäre Teams erforderlich sind.
Die Symptomatik epileptischer Patienten ähnelt oft anderen Neuroentwicklungsstörungen. Daher können Rehabilitationsstrategien aus anderen klinischen Bereichen (kognitive Stimulation, Optimierung oder Kompensation) angewendet werden.
Wichtigster Aspekt in der Intervention ist die Semiotik des Anfalls und seine Entwicklung, da sie kognitives Profil und Verlauf bestimmen.
Epilepsie in anderen Pathologien
Epilepsie tritt auch bei zerebraler Kinderlähmung, genetischen Syndromen, Autismus etc. auf und verschlechtert dort klinische Manifestationen oder verursacht neuropsychologische Regressionen.
Jede wiederkehrende Anfallsform beeinträchtigt kognitive Funktionen, auch als benign geltende kindliche Anfälle. Zwar fehlen initial Symptome, langfristig zeigen sich subtile Defizite (Aufmerksamkeit, Arbeitsgedächtnis, Hemmung). Daher sind auch hier Diagnostik und Monitoring wichtig.
Anforderungen an ein neuropsychologisches Rehabilitationsprogramm bei Epilepsie
Ein neuropsychologisches Rehabilitationsprogramm sollte:
- Auf theoretische Bezugsmodelle zurückgreifen,
- eine interdisziplinäre Perspektive im Umfeld des Kindes (Therapie, Schule, Familie) annehmen,
- Prioritäten klar festlegen,
- Einsatz möglichst früh beginnen,
- ausreichend Therapiedauer (fallabhängig) garantieren,
- auf erhaltene Fähigkeiten aufbauen,
- Emotionale und motivationale Variablen berücksichtigen,
- starke Familienunterstützung einbinden.
Bedeutung der Neurorehabilitation bei Epilepsie
Neurorehabilitation ist nicht nur für kognitive Stimulation und Rehabilita-tion entscheidend, sondern auch, um das kognitive Profil und Anfallsmuster zu verfolgen.
Neuropsychologische Behandlung ermöglicht ein fortlaufendes klinisches Monitoring und schult den Neuropsychologen in der Semiotik einzelner Patienten. So lassen sich subtile klinische Veränderungen oder neue Muster in Anfallsverläufen erkennen, verursacht durch medikamentöse Anpassungen, emotionale Zustände oder Überstimulierung.
Dies erlaubt, kognitive Verschlechterungen oder Krankheitsprogression zu dokumentieren und medikamentöse Anpassungen zu empfehlen, um Nebenwirkungen zu minimieren.
Abschließend sei betont, dass alle Programme (digital oder Papier) lediglich Werkzeuge zur Förderung betroffener Prozesse sind. Erfolg hängt vom definierten Ziel und der Methodik ab.
Kognitive Prozesse sind nicht unabhängig, insbesondere bei netzwerkbasierten Störungen wie Epilepsie. Das menschliche kognitive System beruht auf der Interaktion verschiedener neuropsychologischer Prozesse, die sich in Entwicklung und Erholung gegenseitig beeinflussen. Daher ist es wichtig, keine isolierte Funktionsrehabilitation anzustreben.
Wenn Ihnen dieser Artikel zu Klinischer Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie gefallen hat, könnten Sie auch an folgenden Beiträgen interessiert sein:
Dieser Artikel wurde übersetzt; Link zum Originalartikel auf Spanisch:
Neuropsicología clínica en la neurocirugía de la epilepsia pediátrica
- Oxitocin der Mutter bei Geburt fördert Chlorid-Ausstrom aus fetalen Neuronen und macht GABA inhibitorischer,
- fetales fettreiches Ernährung fördert Ketonkörperbildung mit neuroprotektiver Wirkung.
Ab dem zweiten Lebensjahr verlangsamt sich die Synapsenbildung, die Myelinisierung ist weiter fortgeschritten, wodurch die Epilepsie-Inzidenz sinkt.
Frühe Epilepsie entsteht, wenn schädigende Mechanismen (genetische Defekte, neuronale Migrationsstörungen, entzündliche, infektiöse, traumatische oder tumoröse Ursachen) auf die physiologische Hypererregbarkeit des kindlichen Gehirns einwirken. Sie können an prä- und postsynaptischer Ebene, in der Glia oder an Zelladhäsionsmolekülen wirken und komplex miteinander interagieren.
Störungen synaptischer Proteine führen zu Dysfunktionen neuronaler Schaltkreise und spielen in ätiologischen/lesionalen Mechanismen pädiatrischer Epilepsiesyndrome sowie in Autismus- und Intelligenzminderungs-Erkrankungen eine Rolle.
Genetische Untersuchungen bei kindlicher Epilepsie
Genetische Studien haben Gene aufgedeckt, deren Funktionsverlust neuroentwicklungsstörende Effekte mit oder ohne Epilepsie verursacht.
Beispiel ist das SCN2A-Gen, das die alpha-2-Untereinheit des Natriumkanals codiert. Mutationen können zu variabler Schwere führen:
- Familiäre benign infantile Anfälle (klingen bis zum 2. Lebensjahr ab, ohne Langzeitfolgen),
- Epileptische Enzephalopathie im Säuglingsalter (schwer kontrollierbare Anfälle <1 Jahr, gefolgt von Entwicklungsverzögerung),
- Autismus-Spektrum-Störung, wobei ca. 30 % später Epilepsie entwickeln (nach dem 12. Monat).
Diese genetisch bedingten Epilepsien führten dazu, dass die ILAE 2017 den Begriff „epileptische Enzephalopathie“ auf „Entwicklungs- und epileptische Enzephalopathie“ erweiterte, um Epilepsie uneingeschränkt als Entwicklungsstörung anzuerkennen.
Dies ist ein weiterer Fortschritt in Richtung Anerkennung kindlicher Epilepsie als Neuroentwicklungsstörung, unterstützt von immer mehr Forschungsergebnissen.
Neuropsychologische Diagnostik und Rolle des klinischen Neuropsychologen bei pädiatrischer Epilepsie
Heute gewinnt nicht nur die neuropsychologische Diagnostik von Epilepsiepatienten zunehmend an Bedeutung, sondern auch die Rolle des Neuropsychologen in Epilepsieteams für Diagnostik, chirurgische Intervention und Rehabilitation.
Bei Kindern liefert die neuropsychologische Untersuchung wesentliche Informationen zur Betreuung und Anleitung. Epilepsie kann im sich entwickelnden Gehirn Dysfunktionen in weitreichenden Netzwerken festigen (Fournier, 2019).
Die Ziele der Diagnostik sind diagnostischer Natur: Kognitive oder Verhaltensstörungen liefern wichtige Hinweise zur Lokalisation und Lateralisation der Anfälle, was für die Epilepsiechirurgie sehr hilfreich ist. Zudem unterstützt sie ein besseres Verständnis des Epilepsiesyndroms und damit fundiertere therapeutische Entscheidungen, pharmacologisch und non-pharmacologisch.
Ziele einer neuropsychologischen Untersuchung bei pädiatrischer Epilepsie
Nach Chulune (2010) lassen sich folgende Ziele hervorheben:
- Erfassung eines neuropsychologischen Basisprofils, um Risiken für Entwicklungs-, kognitive, schulische oder psychopathologische Probleme ab dem ersten Anfall zu erkennen.
- Erleichterung der Erkennung neurologischer Störungen, die bei Kindern oft unbemerkt bleiben und als normale Entwicklungsverzögerung fehlgedeutet werden.
- Monitoring kognitiver und Verhaltensänderungen im Krankheitsverlauf.
- Diagnose psychopathologischer Auffälligkeiten und Bewertung ihrer Auswirkung auf Kognition und adaptive Fähigkeiten.
- Unterstützung bei Therapie- und Förderungsplänen und schulischer Maßnahmen.
- Dokumentation möglicher unerwünschter Nebenwirkungen antiepileptischer Medikamente auf kognitiver und verhaltensbezogener Ebene.
Die ILAE empfiehlt, die neuropsychologische Diagnostik als Teil der Routineversorgung von Epilepsiepatienten zu integrieren (Wilson et al., 2015). Der klinische Neuropsychologe sollte weit über Testadministration und statistische Auswertung hinaus aktiv sein, mit umfassender Ausbildung und langjähriger Erfahrung in klinischer und entwicklungsbezogener Neuropsychologie.
Die Analyse der kognitiven Semiotik gewinnt an Bedeutung, um Informationen aus Testverfahren mit der Krankengeschichte und Untersuchung des Patienten zu synthetisieren.
Angesichts der Schwierigkeiten, strukturierte Protokolle bei jungen Kindern mit ausgeprägten Entwicklungsstörungen anzuwenden, ist Anpassungsfähigkeit des Neuropsychologen gefragt, um ein belastbares kognitives Profil zu erstellen.
Neuropsychologische Testprotokolle
Wegen der speziellen Epilepsiefolgen in der Kindheit sind Standardprotokolle, wie bei Erwachsenen, schwer anzuwenden. Internationale und nationale Leitlinien für Kinder existieren kaum.
Wichtig ist, dass man keine noch in Entwicklung befindlichen Funktionen testet. Faktoren wie Aufmerksamkeit, Müdigkeit oder emotionsbedingte Einflüsse sind bei Kindern stärker ausgeprägt. Daher empfiehlt sich Flexibilität, Einführung des Kindes beim Untersucher und Zeitneutralität.
Screening-Tests alleine reichen nicht aus; das Protokoll muss breit genug sein, um verschiedene kognitive Domänen abzudecken. Funktionen wie Gedächtnis sind unter 5 Jahren oft nicht zuverlässig zu prüfen.
Bei exekutiven Funktionen sind verfügbare Tests hoch sensitiv, aber weniger spezifisch, da Sedierung und verlangsamte Informationsverarbeitung durch Antiepileptika viele Ergebnisse sekundär beeinflussen. Somit gewinnen kognitive Semiotik und qualitative Analysen an Bedeutung.
Klinische Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie
Epilepsiechirurgie bei Kindern wird oft nicht als Hauptbehandlungsoption gesehen, sollte aber nicht nur als letzter Schritt bei pharmakoresistenten Fällen betrachtet werden.
Angesichts der Bedeutung des sich entwickelnden Gehirns ist das Hauptziel aller Epilepsiechirurgieteams, die neuroentwicklungsprognose nicht zu verschlechtern. Hierbei ist der Beitrag der Neuropsychologie entscheidend. Der Neuropsychologe ist aktiv bei Auswahl, Evaluation, intraoperativer Betreuung und vor allem postoperativer Anleitung von Familie und Reha-Teams.
Dank fortgeschrittener struktureller und funktioneller Bildgebung lassen sich Kandidaten mit refraktären Läsionen besser erkennen (Berg et al., 2017).
Hauptziele einer neuropsychologischen Untersuchung bei Epilepsiechirurgie
Nach ILAE-Protokoll (Jayakar et al., 2014) sind die Ziele:
- Erstellung einer Basislinie, um Operationsauswirkungen quantitativ zu erfassen,
- Charakterisierung kognitiver Stärken und Defizite, teils vorher unentdeckt,
- Unterstützung bei Lokalisation oder Lateralisation kognitiver Funktionen,
- Information über Risiken postoperativer Defizite,
- Planung von Bildungs- und Rehabilitationsmaßnahmen für Kinder.
Standardpräoperatives Protokoll
- Strukturelles Hochauflösungs-Bildgebungsstudium (3 Tesla MRT),
- Neurophysiologisches Studium mit Video-EEG-Monitoring,
- Komplette neuropsychologische Untersuchung.
Für bestmögliche postoperative Ergebnisse (vollständige Läsionsresektion bei minimalen Funktionseinschränkungen) ist eine exakte Lokalisierung der epileptogenen Zone unerlässlich.
Weshalb es wichtig ist, zwischen symptomatischer Zone (Kortexregion, die durch Entladung Iktalzeichen erzeugt) und irritativer Zone (Region, die interiktale Entladungen generiert und durch EEG/MRT lokalisiert wird) zu unterscheiden.
Entladungen allein erzeugen selten Symptome; meist sind post-entladungsstarke Wellen durch Propagation verantwortlich. Nur selten, wenn Anfälle in eloquenter Zone entstehen, zeigen sich Symptome (Rosenow & Lüders, 2001).
Eine vollständige Läsionsentfernung ist nicht immer nötig und trotz kompletter Resektion können Anfälle persistieren (López & Pomposo-Graztela, 2001). Studien liefern meist nur einen Überblick über Läsionen („Eisbergspitze“), sodass viele finale Resektionsentscheidungen intraoperativ mit direkter Läsionsinformation getroffen werden. Deshalb ist die Präsenz des Neuropsychologen im OP, auch ohne waches Aufwachen, notwendig.
Im pädiatrischen Bereich ist die Rolle des Neuropsychologen noch wichtiger, da er Vertrauen zum Kind aufbaut und die Familie unterstützt.
Hirnplastizität
Die Plastizität im Kindesalter ist entscheidend für die Operationsplanung, nicht nur wegen kognitiver Reorganisation, sondern auch wegen der chronischen Anfallsfolgen in der Neuroentwicklung.
Der neurokognitive Verlauf nach Operation hängt von vielen Faktoren ab:
- Ätiologie der Läsion,
- Alter bei Anfallsbeginn,
- Alter zur OP,
- Interventionsart und Komplikationen,
- medikamentöse Therapie,
- interventionelles Umfeld,
- Zugang zu vorangegangener Neurorehabilitation,
- usw.
Bessere Anfallskontrolle oder Reduktion antiepileptischer Medikamente führt zu deutlicher neurokognitiver Verbesserung.
Die verfügbare Evidenz stammt meist aus Einzelfällen oder kurzen Fallserien. Es bedarf weiterer Dokumentation der neuropsychologischen Entwicklung zur besseren Abwägung von Risiken und Nutzen früher radikaler Eingriffe (Fournier, 2019).
Spezifische Protokolle ähneln den oben genannten, mit Vertiefung in Sprache, Gedächtnis oder visuell-räumliche Funktionen oder Ergänzung psychopatologischer Skalen.
Nachsorge
In der chirurgischen Nachsorge ist es wichtig, das Bewusstsein und grundlegende Funktionen des Kindes beim Aufwachen, in den folgenden Tagen und sechs Monate postoperativ umfassend neuropsychologisch zu bewerten. Ziel ist, Rehabilitations- und Bildungsprogramme festzulegen.
In einigen Fällen (meist 7–8 Jahre) und je nach Läsionslage in eloquenter Zone kann ein intraoperatives Mapping mit wachem Patienten erwogen werden. Hier muss der Neuropsychologe den Patienten im Vorfeld an Tests und Abläufe gewöhnen.
Meist versucht man jedoch, wache intraoperative Protokolle bei Kindern zu vermeiden und greift auf funktionelle MRT oder Wada-Test zurück.
Wenn keine klaren Daten vorliegen oder das Risiko in eloquenter Zone (Sprache, Gedächtnis) hoch ist, ist ein intraoperatives Hirnmapping notwendig. Wann möglich, sollte Monate vor der OP ein longitudinales neuropsychologisches Protokoll erfolgen, um:
- den Patienten longitudinal zu evaluieren,
- Vertrauen zum Kind und der Familie aufzubauen,
- Testtrainings für das intraoperative Mapping durchzuführen.
In dieser Zeit empfiehlt sich ein Programm zur neuropsychologischen Rehabilitation und Stimulation, um bessere prächirurgische, intraoperative Abläufe und eine Reduktion ängstlicher Krisen und posttraumatischer Belastungsreaktionen zu erreichen.
Kognitive Neurorehabilitation bei Epilepsie
Patientenfaktoren für Neurorehabilitationsprogramme
Das neuropsychologische Profil epileptischer Patienten variiert. Für Neurorehabilitation sind folgende Faktoren entscheidend:
1. Alter beim Anfallsbeginn
Das strukturelle und funktionelle Reifealter des Gehirns bestimmt klinische und neurophysiologische Ausdrucksformen. Früher Beginn erhöht Risiko kognitiver Beeinträchtigungen. Studien zeigen, dass das Alter 0–5 Jahre am kritischsten ist (Mauri et al., 2001).
2. Anfallstypen
Generalisierte Anfälle führen normalerweise zu stärkeren kognitiven Beeinträchtigungen als fokale Anfälle.
- Generalisierte Anfälle betreffen tiefe subcorticale Strukturen, Thalamus und retikuläres Formatio-System, die komplexe Funktionen steuern.
- Fokale Epilepsien sind oft mit spezifischen neuropsychologischen Defiziten je nach Anfallslokalisation verbunden (Mulas et al., 2006).
3. Anfallsfrequenz
Häufigere Anfälle beeinträchtigen kognitive Funktionen stärker.
4. Ätiologie oder Epilepsiesyndrom
Epileptische Enzephalopathien (z. B. West, Lennox-Gastaut) haben schlechteste Prognose mit progredienter Beeinträchtigung durch exzessive, diffuse elektrische Aktivität (Nieto, 2011).
5. Pharmakotherapie
Antiepileptika können durch Anfallskontrolle positive kognitive und emotionale Effekte haben, doch sie beeinflussen auch neuronale Netze, die Kognition regulieren, und können unerwünschte neuropsychologische Effekte verursachen.
Moderne Antiepileptika haben geringeren kognitiven Impact, doch zeigt sich in der Praxis weiter eine Beziehung zwischen Medikation und kognitiver Leistung. Beeinträchtigungen sind meist spezifisch und nicht generalisiert.
Monotherapie
Bei zu hohen Blutspiegeln oder rascher Dosissteigerung (Álvarez-Carriles et al., 2011) können auch zwei Medikamente mit geringem kognitiven Nebeneffekt kombinierte Probleme verursachen (Moog, 2009).
Die meisten Antiepileptika reduzieren Membranerregbarkeit, erhöhen postsynaptische Hemmung oder stören Netzsynchronisation. Dies verringert Verarbeitungs- und Aufmerksamkeitsgeschwindigkeit, was in sich entwickelnden Gehirnen stark einschränkend wirken kann.
Allgemeine Nebenwirkungen antiepileptischer Medikamente
Trotz individueller Unterschiede lassen sich folgende Nebenwirkungen festhalten:
- Aufmerksamkeits- und Hemmungsstörungen, verstärkt durch Sedierung oder Schlaflosigkeit,
- Verlangsamung der Informationsverarbeitung,
- Reizbarkeit,
- motorische Unruhe,
- emotionale Dysregulation,
- Beeinträchtigung des Arbeitsgedächtnisses,
- Visusveränderungen,
- usw. (Campos-Castelló & Campos-Soler, 2004).
Größere Defizite finden sich bei pharmakoresistenten Patienten, besonders mit frühem Erkrankungsbeginn, da sie langjährige Chronizität und mehrere Therapien erleben.
Dosis und Anstiegsraten müssen beachtet werden, da kognitive Symptome dosisabhängig zunehmen.
6. Hirnplastizität
Die funktionelle Reorganisation in pädiatrischer Epilepsie zeigt, dass Sprache und Gedächtnis flexibel sind und sich während der Entwicklung verlagern können – etwa von der linken Dominanzregion ins rechte Hemisphären-Pendant oder zu nichttraditionellen Regionen (Brazdil et al., 2005). Dennoch ist dies individuell sehr komplex und erfordert spezialisierte neuropsychologische Rehabilitation.
Diese Faktoren unterscheiden sich je Patient. In Epilepsie sind subkortikale Funktionen (Aufrechterhaltung der Aufmerksamkeit, Arbeitsgedächtnis, Verarbeitungsgeschwindigkeit, kategoriales Abrufen) primär betroffen und verschlechtern sich durch Medikamente zusätzlich.
Klinische und neuropsychologische Manifestationen bei Epilepsie
Primär betroffen sind Aufmerksamkeit, Gedächtnis, Sprache, Verarbeitungsgeschwindigkeit, Hemmung und Arbeitsgedächtnis. Bei entwicklungsbedingten Enzephalopathien ist die Beeinträchtigung umfassender, sodass interdisziplinäre Teams erforderlich sind.
Die Symptomatik epileptischer Patienten ähnelt oft anderen Neuroentwicklungsstörungen. Daher können Rehabilitationsstrategien aus anderen klinischen Bereichen (kognitive Stimulation, Optimierung oder Kompensation) angewendet werden.
Wichtigster Aspekt in der Intervention ist die Semiotik des Anfalls und seine Entwicklung, da sie kognitives Profil und Verlauf bestimmen.
Epilepsie in anderen Pathologien
Epilepsie tritt auch bei zerebraler Kinderlähmung, genetischen Syndromen, Autismus etc. auf und verschlechtert dort klinische Manifestationen oder verursacht neuropsychologische Regressionen.
Jede wiederkehrende Anfallsform beeinträchtigt kognitive Funktionen, auch als benign geltende kindliche Anfälle. Zwar fehlen initial Symptome, langfristig zeigen sich subtile Defizite (Aufmerksamkeit, Arbeitsgedächtnis, Hemmung). Daher sind auch hier Diagnostik und Monitoring wichtig.
Anforderungen an ein neuropsychologisches Rehabilitationsprogramm bei Epilepsie
Ein neuropsychologisches Rehabilitationsprogramm sollte:
- Auf theoretische Bezugsmodelle zurückgreifen,
- eine interdisziplinäre Perspektive im Umfeld des Kindes (Therapie, Schule, Familie) annehmen,
- Prioritäten klar festlegen,
- Einsatz möglichst früh beginnen,
- ausreichend Therapiedauer (fallabhängig) garantieren,
- auf erhaltene Fähigkeiten aufbauen,
- Emotionale und motivationale Variablen berücksichtigen,
- starke Familienunterstützung einbinden.
Bedeutung der Neurorehabilitation bei Epilepsie
Neurorehabilitation ist nicht nur für kognitive Stimulation und Rehabilita-tion entscheidend, sondern auch, um das kognitive Profil und Anfallsmuster zu verfolgen.
Neuropsychologische Behandlung ermöglicht ein fortlaufendes klinisches Monitoring und schult den Neuropsychologen in der Semiotik einzelner Patienten. So lassen sich subtile klinische Veränderungen oder neue Muster in Anfallsverläufen erkennen, verursacht durch medikamentöse Anpassungen, emotionale Zustände oder Überstimulierung.
Dies erlaubt, kognitive Verschlechterungen oder Krankheitsprogression zu dokumentieren und medikamentöse Anpassungen zu empfehlen, um Nebenwirkungen zu minimieren.
Abschließend sei betont, dass alle Programme (digital oder Papier) lediglich Werkzeuge zur Förderung betroffener Prozesse sind. Erfolg hängt vom definierten Ziel und der Methodik ab.
Kognitive Prozesse sind nicht unabhängig, insbesondere bei netzwerkbasierten Störungen wie Epilepsie. Das menschliche kognitive System beruht auf der Interaktion verschiedener neuropsychologischer Prozesse, die sich in Entwicklung und Erholung gegenseitig beeinflussen. Daher ist es wichtig, keine isolierte Funktionsrehabilitation anzustreben.
Wenn Ihnen dieser Artikel zu Klinischer Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie gefallen hat, könnten Sie auch an folgenden Beiträgen interessiert sein:
Dieser Artikel wurde übersetzt; Link zum Originalartikel auf Spanisch:
Neuropsicología clínica en la neurocirugía de la epilepsia pediátrica
- Hohe Konzentrationen neurotropher Faktoren, die neuroprotektiv wirken,
- Glutamatrezyptor-Reuptake-Transporter in Astrozyten,
- Unreife zytotoxische Schutzmechanismen gegen Glutamattoxizität,
- Geringere Konzentration proinflammatorischer Zytokine.
Extrinsische Schutzfaktoren
Weitere äußere Faktoren tragen bei:
- Oxitocin der Mutter bei Geburt fördert Chlorid-Ausstrom aus fetalen Neuronen und macht GABA inhibitorischer,
- fetales fettreiches Ernährung fördert Ketonkörperbildung mit neuroprotektiver Wirkung.
Ab dem zweiten Lebensjahr verlangsamt sich die Synapsenbildung, die Myelinisierung ist weiter fortgeschritten, wodurch die Epilepsie-Inzidenz sinkt.
Frühe Epilepsie entsteht, wenn schädigende Mechanismen (genetische Defekte, neuronale Migrationsstörungen, entzündliche, infektiöse, traumatische oder tumoröse Ursachen) auf die physiologische Hypererregbarkeit des kindlichen Gehirns einwirken. Sie können an prä- und postsynaptischer Ebene, in der Glia oder an Zelladhäsionsmolekülen wirken und komplex miteinander interagieren.
Störungen synaptischer Proteine führen zu Dysfunktionen neuronaler Schaltkreise und spielen in ätiologischen/lesionalen Mechanismen pädiatrischer Epilepsiesyndrome sowie in Autismus- und Intelligenzminderungs-Erkrankungen eine Rolle.
Genetische Untersuchungen bei kindlicher Epilepsie
Genetische Studien haben Gene aufgedeckt, deren Funktionsverlust neuroentwicklungsstörende Effekte mit oder ohne Epilepsie verursacht.
Beispiel ist das SCN2A-Gen, das die alpha-2-Untereinheit des Natriumkanals codiert. Mutationen können zu variabler Schwere führen:
- Familiäre benign infantile Anfälle (klingen bis zum 2. Lebensjahr ab, ohne Langzeitfolgen),
- Epileptische Enzephalopathie im Säuglingsalter (schwer kontrollierbare Anfälle <1 Jahr, gefolgt von Entwicklungsverzögerung),
- Autismus-Spektrum-Störung, wobei ca. 30 % später Epilepsie entwickeln (nach dem 12. Monat).
Diese genetisch bedingten Epilepsien führten dazu, dass die ILAE 2017 den Begriff „epileptische Enzephalopathie“ auf „Entwicklungs- und epileptische Enzephalopathie“ erweiterte, um Epilepsie uneingeschränkt als Entwicklungsstörung anzuerkennen.
Dies ist ein weiterer Fortschritt in Richtung Anerkennung kindlicher Epilepsie als Neuroentwicklungsstörung, unterstützt von immer mehr Forschungsergebnissen.
Neuropsychologische Diagnostik und Rolle des klinischen Neuropsychologen bei pädiatrischer Epilepsie
Heute gewinnt nicht nur die neuropsychologische Diagnostik von Epilepsiepatienten zunehmend an Bedeutung, sondern auch die Rolle des Neuropsychologen in Epilepsieteams für Diagnostik, chirurgische Intervention und Rehabilitation.
Bei Kindern liefert die neuropsychologische Untersuchung wesentliche Informationen zur Betreuung und Anleitung. Epilepsie kann im sich entwickelnden Gehirn Dysfunktionen in weitreichenden Netzwerken festigen (Fournier, 2019).
Die Ziele der Diagnostik sind diagnostischer Natur: Kognitive oder Verhaltensstörungen liefern wichtige Hinweise zur Lokalisation und Lateralisation der Anfälle, was für die Epilepsiechirurgie sehr hilfreich ist. Zudem unterstützt sie ein besseres Verständnis des Epilepsiesyndroms und damit fundiertere therapeutische Entscheidungen, pharmacologisch und non-pharmacologisch.
Ziele einer neuropsychologischen Untersuchung bei pädiatrischer Epilepsie
Nach Chulune (2010) lassen sich folgende Ziele hervorheben:
- Erfassung eines neuropsychologischen Basisprofils, um Risiken für Entwicklungs-, kognitive, schulische oder psychopathologische Probleme ab dem ersten Anfall zu erkennen.
- Erleichterung der Erkennung neurologischer Störungen, die bei Kindern oft unbemerkt bleiben und als normale Entwicklungsverzögerung fehlgedeutet werden.
- Monitoring kognitiver und Verhaltensänderungen im Krankheitsverlauf.
- Diagnose psychopathologischer Auffälligkeiten und Bewertung ihrer Auswirkung auf Kognition und adaptive Fähigkeiten.
- Unterstützung bei Therapie- und Förderungsplänen und schulischer Maßnahmen.
- Dokumentation möglicher unerwünschter Nebenwirkungen antiepileptischer Medikamente auf kognitiver und verhaltensbezogener Ebene.
Die ILAE empfiehlt, die neuropsychologische Diagnostik als Teil der Routineversorgung von Epilepsiepatienten zu integrieren (Wilson et al., 2015). Der klinische Neuropsychologe sollte weit über Testadministration und statistische Auswertung hinaus aktiv sein, mit umfassender Ausbildung und langjähriger Erfahrung in klinischer und entwicklungsbezogener Neuropsychologie.
Die Analyse der kognitiven Semiotik gewinnt an Bedeutung, um Informationen aus Testverfahren mit der Krankengeschichte und Untersuchung des Patienten zu synthetisieren.
Angesichts der Schwierigkeiten, strukturierte Protokolle bei jungen Kindern mit ausgeprägten Entwicklungsstörungen anzuwenden, ist Anpassungsfähigkeit des Neuropsychologen gefragt, um ein belastbares kognitives Profil zu erstellen.
Neuropsychologische Testprotokolle
Wegen der speziellen Epilepsiefolgen in der Kindheit sind Standardprotokolle, wie bei Erwachsenen, schwer anzuwenden. Internationale und nationale Leitlinien für Kinder existieren kaum.
Wichtig ist, dass man keine noch in Entwicklung befindlichen Funktionen testet. Faktoren wie Aufmerksamkeit, Müdigkeit oder emotionsbedingte Einflüsse sind bei Kindern stärker ausgeprägt. Daher empfiehlt sich Flexibilität, Einführung des Kindes beim Untersucher und Zeitneutralität.
Screening-Tests alleine reichen nicht aus; das Protokoll muss breit genug sein, um verschiedene kognitive Domänen abzudecken. Funktionen wie Gedächtnis sind unter 5 Jahren oft nicht zuverlässig zu prüfen.
Bei exekutiven Funktionen sind verfügbare Tests hoch sensitiv, aber weniger spezifisch, da Sedierung und verlangsamte Informationsverarbeitung durch Antiepileptika viele Ergebnisse sekundär beeinflussen. Somit gewinnen kognitive Semiotik und qualitative Analysen an Bedeutung.
Klinische Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie
Epilepsiechirurgie bei Kindern wird oft nicht als Hauptbehandlungsoption gesehen, sollte aber nicht nur als letzter Schritt bei pharmakoresistenten Fällen betrachtet werden.
Angesichts der Bedeutung des sich entwickelnden Gehirns ist das Hauptziel aller Epilepsiechirurgieteams, die neuroentwicklungsprognose nicht zu verschlechtern. Hierbei ist der Beitrag der Neuropsychologie entscheidend. Der Neuropsychologe ist aktiv bei Auswahl, Evaluation, intraoperativer Betreuung und vor allem postoperativer Anleitung von Familie und Reha-Teams.
Dank fortgeschrittener struktureller und funktioneller Bildgebung lassen sich Kandidaten mit refraktären Läsionen besser erkennen (Berg et al., 2017).
Hauptziele einer neuropsychologischen Untersuchung bei Epilepsiechirurgie
Nach ILAE-Protokoll (Jayakar et al., 2014) sind die Ziele:
- Erstellung einer Basislinie, um Operationsauswirkungen quantitativ zu erfassen,
- Charakterisierung kognitiver Stärken und Defizite, teils vorher unentdeckt,
- Unterstützung bei Lokalisation oder Lateralisation kognitiver Funktionen,
- Information über Risiken postoperativer Defizite,
- Planung von Bildungs- und Rehabilitationsmaßnahmen für Kinder.
Standardpräoperatives Protokoll
- Strukturelles Hochauflösungs-Bildgebungsstudium (3 Tesla MRT),
- Neurophysiologisches Studium mit Video-EEG-Monitoring,
- Komplette neuropsychologische Untersuchung.
Für bestmögliche postoperative Ergebnisse (vollständige Läsionsresektion bei minimalen Funktionseinschränkungen) ist eine exakte Lokalisierung der epileptogenen Zone unerlässlich.
Weshalb es wichtig ist, zwischen symptomatischer Zone (Kortexregion, die durch Entladung Iktalzeichen erzeugt) und irritativer Zone (Region, die interiktale Entladungen generiert und durch EEG/MRT lokalisiert wird) zu unterscheiden.
Entladungen allein erzeugen selten Symptome; meist sind post-entladungsstarke Wellen durch Propagation verantwortlich. Nur selten, wenn Anfälle in eloquenter Zone entstehen, zeigen sich Symptome (Rosenow & Lüders, 2001).
Eine vollständige Läsionsentfernung ist nicht immer nötig und trotz kompletter Resektion können Anfälle persistieren (López & Pomposo-Graztela, 2001). Studien liefern meist nur einen Überblick über Läsionen („Eisbergspitze“), sodass viele finale Resektionsentscheidungen intraoperativ mit direkter Läsionsinformation getroffen werden. Deshalb ist die Präsenz des Neuropsychologen im OP, auch ohne waches Aufwachen, notwendig.
Im pädiatrischen Bereich ist die Rolle des Neuropsychologen noch wichtiger, da er Vertrauen zum Kind aufbaut und die Familie unterstützt.
Hirnplastizität
Die Plastizität im Kindesalter ist entscheidend für die Operationsplanung, nicht nur wegen kognitiver Reorganisation, sondern auch wegen der chronischen Anfallsfolgen in der Neuroentwicklung.
Der neurokognitive Verlauf nach Operation hängt von vielen Faktoren ab:
- Ätiologie der Läsion,
- Alter bei Anfallsbeginn,
- Alter zur OP,
- Interventionsart und Komplikationen,
- medikamentöse Therapie,
- interventionelles Umfeld,
- Zugang zu vorangegangener Neurorehabilitation,
- usw.
Bessere Anfallskontrolle oder Reduktion antiepileptischer Medikamente führt zu deutlicher neurokognitiver Verbesserung.
Die verfügbare Evidenz stammt meist aus Einzelfällen oder kurzen Fallserien. Es bedarf weiterer Dokumentation der neuropsychologischen Entwicklung zur besseren Abwägung von Risiken und Nutzen früher radikaler Eingriffe (Fournier, 2019).
Spezifische Protokolle ähneln den oben genannten, mit Vertiefung in Sprache, Gedächtnis oder visuell-räumliche Funktionen oder Ergänzung psychopatologischer Skalen.
Nachsorge
In der chirurgischen Nachsorge ist es wichtig, das Bewusstsein und grundlegende Funktionen des Kindes beim Aufwachen, in den folgenden Tagen und sechs Monate postoperativ umfassend neuropsychologisch zu bewerten. Ziel ist, Rehabilitations- und Bildungsprogramme festzulegen.
In einigen Fällen (meist 7–8 Jahre) und je nach Läsionslage in eloquenter Zone kann ein intraoperatives Mapping mit wachem Patienten erwogen werden. Hier muss der Neuropsychologe den Patienten im Vorfeld an Tests und Abläufe gewöhnen.
Meist versucht man jedoch, wache intraoperative Protokolle bei Kindern zu vermeiden und greift auf funktionelle MRT oder Wada-Test zurück.
Wenn keine klaren Daten vorliegen oder das Risiko in eloquenter Zone (Sprache, Gedächtnis) hoch ist, ist ein intraoperatives Hirnmapping notwendig. Wann möglich, sollte Monate vor der OP ein longitudinales neuropsychologisches Protokoll erfolgen, um:
- den Patienten longitudinal zu evaluieren,
- Vertrauen zum Kind und der Familie aufzubauen,
- Testtrainings für das intraoperative Mapping durchzuführen.
In dieser Zeit empfiehlt sich ein Programm zur neuropsychologischen Rehabilitation und Stimulation, um bessere prächirurgische, intraoperative Abläufe und eine Reduktion ängstlicher Krisen und posttraumatischer Belastungsreaktionen zu erreichen.
Kognitive Neurorehabilitation bei Epilepsie
Patientenfaktoren für Neurorehabilitationsprogramme
Das neuropsychologische Profil epileptischer Patienten variiert. Für Neurorehabilitation sind folgende Faktoren entscheidend:
1. Alter beim Anfallsbeginn
Das strukturelle und funktionelle Reifealter des Gehirns bestimmt klinische und neurophysiologische Ausdrucksformen. Früher Beginn erhöht Risiko kognitiver Beeinträchtigungen. Studien zeigen, dass das Alter 0–5 Jahre am kritischsten ist (Mauri et al., 2001).
2. Anfallstypen
Generalisierte Anfälle führen normalerweise zu stärkeren kognitiven Beeinträchtigungen als fokale Anfälle.
- Generalisierte Anfälle betreffen tiefe subcorticale Strukturen, Thalamus und retikuläres Formatio-System, die komplexe Funktionen steuern.
- Fokale Epilepsien sind oft mit spezifischen neuropsychologischen Defiziten je nach Anfallslokalisation verbunden (Mulas et al., 2006).
3. Anfallsfrequenz
Häufigere Anfälle beeinträchtigen kognitive Funktionen stärker.
4. Ätiologie oder Epilepsiesyndrom
Epileptische Enzephalopathien (z. B. West, Lennox-Gastaut) haben schlechteste Prognose mit progredienter Beeinträchtigung durch exzessive, diffuse elektrische Aktivität (Nieto, 2011).
5. Pharmakotherapie
Antiepileptika können durch Anfallskontrolle positive kognitive und emotionale Effekte haben, doch sie beeinflussen auch neuronale Netze, die Kognition regulieren, und können unerwünschte neuropsychologische Effekte verursachen.
Moderne Antiepileptika haben geringeren kognitiven Impact, doch zeigt sich in der Praxis weiter eine Beziehung zwischen Medikation und kognitiver Leistung. Beeinträchtigungen sind meist spezifisch und nicht generalisiert.
Monotherapie
Bei zu hohen Blutspiegeln oder rascher Dosissteigerung (Álvarez-Carriles et al., 2011) können auch zwei Medikamente mit geringem kognitiven Nebeneffekt kombinierte Probleme verursachen (Moog, 2009).
Die meisten Antiepileptika reduzieren Membranerregbarkeit, erhöhen postsynaptische Hemmung oder stören Netzsynchronisation. Dies verringert Verarbeitungs- und Aufmerksamkeitsgeschwindigkeit, was in sich entwickelnden Gehirnen stark einschränkend wirken kann.
Allgemeine Nebenwirkungen antiepileptischer Medikamente
Trotz individueller Unterschiede lassen sich folgende Nebenwirkungen festhalten:
- Aufmerksamkeits- und Hemmungsstörungen, verstärkt durch Sedierung oder Schlaflosigkeit,
- Verlangsamung der Informationsverarbeitung,
- Reizbarkeit,
- motorische Unruhe,
- emotionale Dysregulation,
- Beeinträchtigung des Arbeitsgedächtnisses,
- Visusveränderungen,
- usw. (Campos-Castelló & Campos-Soler, 2004).
Größere Defizite finden sich bei pharmakoresistenten Patienten, besonders mit frühem Erkrankungsbeginn, da sie langjährige Chronizität und mehrere Therapien erleben.
Dosis und Anstiegsraten müssen beachtet werden, da kognitive Symptome dosisabhängig zunehmen.
6. Hirnplastizität
Die funktionelle Reorganisation in pädiatrischer Epilepsie zeigt, dass Sprache und Gedächtnis flexibel sind und sich während der Entwicklung verlagern können – etwa von der linken Dominanzregion ins rechte Hemisphären-Pendant oder zu nichttraditionellen Regionen (Brazdil et al., 2005). Dennoch ist dies individuell sehr komplex und erfordert spezialisierte neuropsychologische Rehabilitation.
Diese Faktoren unterscheiden sich je Patient. In Epilepsie sind subkortikale Funktionen (Aufrechterhaltung der Aufmerksamkeit, Arbeitsgedächtnis, Verarbeitungsgeschwindigkeit, kategoriales Abrufen) primär betroffen und verschlechtern sich durch Medikamente zusätzlich.
Klinische und neuropsychologische Manifestationen bei Epilepsie
Primär betroffen sind Aufmerksamkeit, Gedächtnis, Sprache, Verarbeitungsgeschwindigkeit, Hemmung und Arbeitsgedächtnis. Bei entwicklungsbedingten Enzephalopathien ist die Beeinträchtigung umfassender, sodass interdisziplinäre Teams erforderlich sind.
Die Symptomatik epileptischer Patienten ähnelt oft anderen Neuroentwicklungsstörungen. Daher können Rehabilitationsstrategien aus anderen klinischen Bereichen (kognitive Stimulation, Optimierung oder Kompensation) angewendet werden.
Wichtigster Aspekt in der Intervention ist die Semiotik des Anfalls und seine Entwicklung, da sie kognitives Profil und Verlauf bestimmen.
Epilepsie in anderen Pathologien
Epilepsie tritt auch bei zerebraler Kinderlähmung, genetischen Syndromen, Autismus etc. auf und verschlechtert dort klinische Manifestationen oder verursacht neuropsychologische Regressionen.
Jede wiederkehrende Anfallsform beeinträchtigt kognitive Funktionen, auch als benign geltende kindliche Anfälle. Zwar fehlen initial Symptome, langfristig zeigen sich subtile Defizite (Aufmerksamkeit, Arbeitsgedächtnis, Hemmung). Daher sind auch hier Diagnostik und Monitoring wichtig.
Anforderungen an ein neuropsychologisches Rehabilitationsprogramm bei Epilepsie
Ein neuropsychologisches Rehabilitationsprogramm sollte:
- Auf theoretische Bezugsmodelle zurückgreifen,
- eine interdisziplinäre Perspektive im Umfeld des Kindes (Therapie, Schule, Familie) annehmen,
- Prioritäten klar festlegen,
- Einsatz möglichst früh beginnen,
- ausreichend Therapiedauer (fallabhängig) garantieren,
- auf erhaltene Fähigkeiten aufbauen,
- Emotionale und motivationale Variablen berücksichtigen,
- starke Familienunterstützung einbinden.
Bedeutung der Neurorehabilitation bei Epilepsie
Neurorehabilitation ist nicht nur für kognitive Stimulation und Rehabilita-tion entscheidend, sondern auch, um das kognitive Profil und Anfallsmuster zu verfolgen.
Neuropsychologische Behandlung ermöglicht ein fortlaufendes klinisches Monitoring und schult den Neuropsychologen in der Semiotik einzelner Patienten. So lassen sich subtile klinische Veränderungen oder neue Muster in Anfallsverläufen erkennen, verursacht durch medikamentöse Anpassungen, emotionale Zustände oder Überstimulierung.
Dies erlaubt, kognitive Verschlechterungen oder Krankheitsprogression zu dokumentieren und medikamentöse Anpassungen zu empfehlen, um Nebenwirkungen zu minimieren.
Abschließend sei betont, dass alle Programme (digital oder Papier) lediglich Werkzeuge zur Förderung betroffener Prozesse sind. Erfolg hängt vom definierten Ziel und der Methodik ab.
Kognitive Prozesse sind nicht unabhängig, insbesondere bei netzwerkbasierten Störungen wie Epilepsie. Das menschliche kognitive System beruht auf der Interaktion verschiedener neuropsychologischer Prozesse, die sich in Entwicklung und Erholung gegenseitig beeinflussen. Daher ist es wichtig, keine isolierte Funktionsrehabilitation anzustreben.
Wenn Ihnen dieser Artikel zu Klinischer Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie gefallen hat, könnten Sie auch an folgenden Beiträgen interessiert sein:
Dieser Artikel wurde übersetzt; Link zum Originalartikel auf Spanisch:
Neuropsicología clínica en la neurocirugía de la epilepsia pediátrica
- Perisylvischer Bereich – ab Geburt,
- Parieto-okzipital – bis 3–7 Monate,
- Prämotorisch-frontal – von 12 Monaten bis ins erste Jahrzehnt.
Parallel verläuft die Myelinisierung kaudal-rostral.
Dies prägt die Semiotik neonataler und infantiler Anfälle, zusätzlich beeinflusst durch hemisphärische Spezialisierung und Entwicklung langer Bahnen.
Für Wachstum, Schaltungsaufbau und -modifikation müssen kindliche Neuronen leicht erregbar sein: GABA wirkt exzitatorisch und Glutamatrezeptoren sind reichlich vorhanden.
Im ersten Lebensjahr dominieren Synaptogenese und Vernetzungsprozesse: Etwa 1000 neue Synapsen pro Sekunde bilden sich, feuern und synchronisieren sich.
Reizübertragung im unreifen Gehirn ist vorrangig exzitatorisch: GABA-Rezeptoren fördern Chlorid-Einstrom und es gibt viele Glutamatrezeptoren. Formende neuronale Schaltkreise haben höhere intrinsische Leitfähigkeit und feuern periodisch, was neue Netze synchronisiert. Dieses exzitatorische Milieu begünstigt Wachstum und Lernen, aber auch epileptische Mechanismen.
Schutzfaktoren gegen Hypererregbarkeit
Intrinsische Schutzfaktoren
Obwohl das kindliche Gehirn hypererregbar ist, tritt Epilepsie nur bei 1–2 % der Unter-Zweijährigen auf, da es über Schutzmechanismen verfügt:
- Hohe Konzentrationen neurotropher Faktoren, die neuroprotektiv wirken,
- Glutamatrezyptor-Reuptake-Transporter in Astrozyten,
- Unreife zytotoxische Schutzmechanismen gegen Glutamattoxizität,
- Geringere Konzentration proinflammatorischer Zytokine.
Extrinsische Schutzfaktoren
Weitere äußere Faktoren tragen bei:
- Oxitocin der Mutter bei Geburt fördert Chlorid-Ausstrom aus fetalen Neuronen und macht GABA inhibitorischer,
- fetales fettreiches Ernährung fördert Ketonkörperbildung mit neuroprotektiver Wirkung.
Ab dem zweiten Lebensjahr verlangsamt sich die Synapsenbildung, die Myelinisierung ist weiter fortgeschritten, wodurch die Epilepsie-Inzidenz sinkt.
Frühe Epilepsie entsteht, wenn schädigende Mechanismen (genetische Defekte, neuronale Migrationsstörungen, entzündliche, infektiöse, traumatische oder tumoröse Ursachen) auf die physiologische Hypererregbarkeit des kindlichen Gehirns einwirken. Sie können an prä- und postsynaptischer Ebene, in der Glia oder an Zelladhäsionsmolekülen wirken und komplex miteinander interagieren.
Störungen synaptischer Proteine führen zu Dysfunktionen neuronaler Schaltkreise und spielen in ätiologischen/lesionalen Mechanismen pädiatrischer Epilepsiesyndrome sowie in Autismus- und Intelligenzminderungs-Erkrankungen eine Rolle.
Genetische Untersuchungen bei kindlicher Epilepsie
Genetische Studien haben Gene aufgedeckt, deren Funktionsverlust neuroentwicklungsstörende Effekte mit oder ohne Epilepsie verursacht.
Beispiel ist das SCN2A-Gen, das die alpha-2-Untereinheit des Natriumkanals codiert. Mutationen können zu variabler Schwere führen:
- Familiäre benign infantile Anfälle (klingen bis zum 2. Lebensjahr ab, ohne Langzeitfolgen),
- Epileptische Enzephalopathie im Säuglingsalter (schwer kontrollierbare Anfälle <1 Jahr, gefolgt von Entwicklungsverzögerung),
- Autismus-Spektrum-Störung, wobei ca. 30 % später Epilepsie entwickeln (nach dem 12. Monat).
Diese genetisch bedingten Epilepsien führten dazu, dass die ILAE 2017 den Begriff „epileptische Enzephalopathie“ auf „Entwicklungs- und epileptische Enzephalopathie“ erweiterte, um Epilepsie uneingeschränkt als Entwicklungsstörung anzuerkennen.
Dies ist ein weiterer Fortschritt in Richtung Anerkennung kindlicher Epilepsie als Neuroentwicklungsstörung, unterstützt von immer mehr Forschungsergebnissen.
Neuropsychologische Diagnostik und Rolle des klinischen Neuropsychologen bei pädiatrischer Epilepsie
Heute gewinnt nicht nur die neuropsychologische Diagnostik von Epilepsiepatienten zunehmend an Bedeutung, sondern auch die Rolle des Neuropsychologen in Epilepsieteams für Diagnostik, chirurgische Intervention und Rehabilitation.
Bei Kindern liefert die neuropsychologische Untersuchung wesentliche Informationen zur Betreuung und Anleitung. Epilepsie kann im sich entwickelnden Gehirn Dysfunktionen in weitreichenden Netzwerken festigen (Fournier, 2019).
Die Ziele der Diagnostik sind diagnostischer Natur: Kognitive oder Verhaltensstörungen liefern wichtige Hinweise zur Lokalisation und Lateralisation der Anfälle, was für die Epilepsiechirurgie sehr hilfreich ist. Zudem unterstützt sie ein besseres Verständnis des Epilepsiesyndroms und damit fundiertere therapeutische Entscheidungen, pharmacologisch und non-pharmacologisch.
Ziele einer neuropsychologischen Untersuchung bei pädiatrischer Epilepsie
Nach Chulune (2010) lassen sich folgende Ziele hervorheben:
- Erfassung eines neuropsychologischen Basisprofils, um Risiken für Entwicklungs-, kognitive, schulische oder psychopathologische Probleme ab dem ersten Anfall zu erkennen.
- Erleichterung der Erkennung neurologischer Störungen, die bei Kindern oft unbemerkt bleiben und als normale Entwicklungsverzögerung fehlgedeutet werden.
- Monitoring kognitiver und Verhaltensänderungen im Krankheitsverlauf.
- Diagnose psychopathologischer Auffälligkeiten und Bewertung ihrer Auswirkung auf Kognition und adaptive Fähigkeiten.
- Unterstützung bei Therapie- und Förderungsplänen und schulischer Maßnahmen.
- Dokumentation möglicher unerwünschter Nebenwirkungen antiepileptischer Medikamente auf kognitiver und verhaltensbezogener Ebene.
Die ILAE empfiehlt, die neuropsychologische Diagnostik als Teil der Routineversorgung von Epilepsiepatienten zu integrieren (Wilson et al., 2015). Der klinische Neuropsychologe sollte weit über Testadministration und statistische Auswertung hinaus aktiv sein, mit umfassender Ausbildung und langjähriger Erfahrung in klinischer und entwicklungsbezogener Neuropsychologie.
Die Analyse der kognitiven Semiotik gewinnt an Bedeutung, um Informationen aus Testverfahren mit der Krankengeschichte und Untersuchung des Patienten zu synthetisieren.
Angesichts der Schwierigkeiten, strukturierte Protokolle bei jungen Kindern mit ausgeprägten Entwicklungsstörungen anzuwenden, ist Anpassungsfähigkeit des Neuropsychologen gefragt, um ein belastbares kognitives Profil zu erstellen.
Neuropsychologische Testprotokolle
Wegen der speziellen Epilepsiefolgen in der Kindheit sind Standardprotokolle, wie bei Erwachsenen, schwer anzuwenden. Internationale und nationale Leitlinien für Kinder existieren kaum.
Wichtig ist, dass man keine noch in Entwicklung befindlichen Funktionen testet. Faktoren wie Aufmerksamkeit, Müdigkeit oder emotionsbedingte Einflüsse sind bei Kindern stärker ausgeprägt. Daher empfiehlt sich Flexibilität, Einführung des Kindes beim Untersucher und Zeitneutralität.
Screening-Tests alleine reichen nicht aus; das Protokoll muss breit genug sein, um verschiedene kognitive Domänen abzudecken. Funktionen wie Gedächtnis sind unter 5 Jahren oft nicht zuverlässig zu prüfen.
Bei exekutiven Funktionen sind verfügbare Tests hoch sensitiv, aber weniger spezifisch, da Sedierung und verlangsamte Informationsverarbeitung durch Antiepileptika viele Ergebnisse sekundär beeinflussen. Somit gewinnen kognitive Semiotik und qualitative Analysen an Bedeutung.
Klinische Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie
Epilepsiechirurgie bei Kindern wird oft nicht als Hauptbehandlungsoption gesehen, sollte aber nicht nur als letzter Schritt bei pharmakoresistenten Fällen betrachtet werden.
Angesichts der Bedeutung des sich entwickelnden Gehirns ist das Hauptziel aller Epilepsiechirurgieteams, die neuroentwicklungsprognose nicht zu verschlechtern. Hierbei ist der Beitrag der Neuropsychologie entscheidend. Der Neuropsychologe ist aktiv bei Auswahl, Evaluation, intraoperativer Betreuung und vor allem postoperativer Anleitung von Familie und Reha-Teams.
Dank fortgeschrittener struktureller und funktioneller Bildgebung lassen sich Kandidaten mit refraktären Läsionen besser erkennen (Berg et al., 2017).
Hauptziele einer neuropsychologischen Untersuchung bei Epilepsiechirurgie
Nach ILAE-Protokoll (Jayakar et al., 2014) sind die Ziele:
- Erstellung einer Basislinie, um Operationsauswirkungen quantitativ zu erfassen,
- Charakterisierung kognitiver Stärken und Defizite, teils vorher unentdeckt,
- Unterstützung bei Lokalisation oder Lateralisation kognitiver Funktionen,
- Information über Risiken postoperativer Defizite,
- Planung von Bildungs- und Rehabilitationsmaßnahmen für Kinder.
Standardpräoperatives Protokoll
- Strukturelles Hochauflösungs-Bildgebungsstudium (3 Tesla MRT),
- Neurophysiologisches Studium mit Video-EEG-Monitoring,
- Komplette neuropsychologische Untersuchung.
Für bestmögliche postoperative Ergebnisse (vollständige Läsionsresektion bei minimalen Funktionseinschränkungen) ist eine exakte Lokalisierung der epileptogenen Zone unerlässlich.
Weshalb es wichtig ist, zwischen symptomatischer Zone (Kortexregion, die durch Entladung Iktalzeichen erzeugt) und irritativer Zone (Region, die interiktale Entladungen generiert und durch EEG/MRT lokalisiert wird) zu unterscheiden.
Entladungen allein erzeugen selten Symptome; meist sind post-entladungsstarke Wellen durch Propagation verantwortlich. Nur selten, wenn Anfälle in eloquenter Zone entstehen, zeigen sich Symptome (Rosenow & Lüders, 2001).
Eine vollständige Läsionsentfernung ist nicht immer nötig und trotz kompletter Resektion können Anfälle persistieren (López & Pomposo-Graztela, 2001). Studien liefern meist nur einen Überblick über Läsionen („Eisbergspitze“), sodass viele finale Resektionsentscheidungen intraoperativ mit direkter Läsionsinformation getroffen werden. Deshalb ist die Präsenz des Neuropsychologen im OP, auch ohne waches Aufwachen, notwendig.
Im pädiatrischen Bereich ist die Rolle des Neuropsychologen noch wichtiger, da er Vertrauen zum Kind aufbaut und die Familie unterstützt.
Hirnplastizität
Die Plastizität im Kindesalter ist entscheidend für die Operationsplanung, nicht nur wegen kognitiver Reorganisation, sondern auch wegen der chronischen Anfallsfolgen in der Neuroentwicklung.
Der neurokognitive Verlauf nach Operation hängt von vielen Faktoren ab:
- Ätiologie der Läsion,
- Alter bei Anfallsbeginn,
- Alter zur OP,
- Interventionsart und Komplikationen,
- medikamentöse Therapie,
- interventionelles Umfeld,
- Zugang zu vorangegangener Neurorehabilitation,
- usw.
Bessere Anfallskontrolle oder Reduktion antiepileptischer Medikamente führt zu deutlicher neurokognitiver Verbesserung.
Die verfügbare Evidenz stammt meist aus Einzelfällen oder kurzen Fallserien. Es bedarf weiterer Dokumentation der neuropsychologischen Entwicklung zur besseren Abwägung von Risiken und Nutzen früher radikaler Eingriffe (Fournier, 2019).
Spezifische Protokolle ähneln den oben genannten, mit Vertiefung in Sprache, Gedächtnis oder visuell-räumliche Funktionen oder Ergänzung psychopatologischer Skalen.
Nachsorge
In der chirurgischen Nachsorge ist es wichtig, das Bewusstsein und grundlegende Funktionen des Kindes beim Aufwachen, in den folgenden Tagen und sechs Monate postoperativ umfassend neuropsychologisch zu bewerten. Ziel ist, Rehabilitations- und Bildungsprogramme festzulegen.
In einigen Fällen (meist 7–8 Jahre) und je nach Läsionslage in eloquenter Zone kann ein intraoperatives Mapping mit wachem Patienten erwogen werden. Hier muss der Neuropsychologe den Patienten im Vorfeld an Tests und Abläufe gewöhnen.
Meist versucht man jedoch, wache intraoperative Protokolle bei Kindern zu vermeiden und greift auf funktionelle MRT oder Wada-Test zurück.
Wenn keine klaren Daten vorliegen oder das Risiko in eloquenter Zone (Sprache, Gedächtnis) hoch ist, ist ein intraoperatives Hirnmapping notwendig. Wann möglich, sollte Monate vor der OP ein longitudinales neuropsychologisches Protokoll erfolgen, um:
- den Patienten longitudinal zu evaluieren,
- Vertrauen zum Kind und der Familie aufzubauen,
- Testtrainings für das intraoperative Mapping durchzuführen.
In dieser Zeit empfiehlt sich ein Programm zur neuropsychologischen Rehabilitation und Stimulation, um bessere prächirurgische, intraoperative Abläufe und eine Reduktion ängstlicher Krisen und posttraumatischer Belastungsreaktionen zu erreichen.
Kognitive Neurorehabilitation bei Epilepsie
Patientenfaktoren für Neurorehabilitationsprogramme
Das neuropsychologische Profil epileptischer Patienten variiert. Für Neurorehabilitation sind folgende Faktoren entscheidend:
1. Alter beim Anfallsbeginn
Das strukturelle und funktionelle Reifealter des Gehirns bestimmt klinische und neurophysiologische Ausdrucksformen. Früher Beginn erhöht Risiko kognitiver Beeinträchtigungen. Studien zeigen, dass das Alter 0–5 Jahre am kritischsten ist (Mauri et al., 2001).
2. Anfallstypen
Generalisierte Anfälle führen normalerweise zu stärkeren kognitiven Beeinträchtigungen als fokale Anfälle.
- Generalisierte Anfälle betreffen tiefe subcorticale Strukturen, Thalamus und retikuläres Formatio-System, die komplexe Funktionen steuern.
- Fokale Epilepsien sind oft mit spezifischen neuropsychologischen Defiziten je nach Anfallslokalisation verbunden (Mulas et al., 2006).
3. Anfallsfrequenz
Häufigere Anfälle beeinträchtigen kognitive Funktionen stärker.
4. Ätiologie oder Epilepsiesyndrom
Epileptische Enzephalopathien (z. B. West, Lennox-Gastaut) haben schlechteste Prognose mit progredienter Beeinträchtigung durch exzessive, diffuse elektrische Aktivität (Nieto, 2011).
5. Pharmakotherapie
Antiepileptika können durch Anfallskontrolle positive kognitive und emotionale Effekte haben, doch sie beeinflussen auch neuronale Netze, die Kognition regulieren, und können unerwünschte neuropsychologische Effekte verursachen.
Moderne Antiepileptika haben geringeren kognitiven Impact, doch zeigt sich in der Praxis weiter eine Beziehung zwischen Medikation und kognitiver Leistung. Beeinträchtigungen sind meist spezifisch und nicht generalisiert.
Monotherapie
Bei zu hohen Blutspiegeln oder rascher Dosissteigerung (Álvarez-Carriles et al., 2011) können auch zwei Medikamente mit geringem kognitiven Nebeneffekt kombinierte Probleme verursachen (Moog, 2009).
Die meisten Antiepileptika reduzieren Membranerregbarkeit, erhöhen postsynaptische Hemmung oder stören Netzsynchronisation. Dies verringert Verarbeitungs- und Aufmerksamkeitsgeschwindigkeit, was in sich entwickelnden Gehirnen stark einschränkend wirken kann.
Allgemeine Nebenwirkungen antiepileptischer Medikamente
Trotz individueller Unterschiede lassen sich folgende Nebenwirkungen festhalten:
- Aufmerksamkeits- und Hemmungsstörungen, verstärkt durch Sedierung oder Schlaflosigkeit,
- Verlangsamung der Informationsverarbeitung,
- Reizbarkeit,
- motorische Unruhe,
- emotionale Dysregulation,
- Beeinträchtigung des Arbeitsgedächtnisses,
- Visusveränderungen,
- usw. (Campos-Castelló & Campos-Soler, 2004).
Größere Defizite finden sich bei pharmakoresistenten Patienten, besonders mit frühem Erkrankungsbeginn, da sie langjährige Chronizität und mehrere Therapien erleben.
Dosis und Anstiegsraten müssen beachtet werden, da kognitive Symptome dosisabhängig zunehmen.
6. Hirnplastizität
Die funktionelle Reorganisation in pädiatrischer Epilepsie zeigt, dass Sprache und Gedächtnis flexibel sind und sich während der Entwicklung verlagern können – etwa von der linken Dominanzregion ins rechte Hemisphären-Pendant oder zu nichttraditionellen Regionen (Brazdil et al., 2005). Dennoch ist dies individuell sehr komplex und erfordert spezialisierte neuropsychologische Rehabilitation.
Diese Faktoren unterscheiden sich je Patient. In Epilepsie sind subkortikale Funktionen (Aufrechterhaltung der Aufmerksamkeit, Arbeitsgedächtnis, Verarbeitungsgeschwindigkeit, kategoriales Abrufen) primär betroffen und verschlechtern sich durch Medikamente zusätzlich.
Klinische und neuropsychologische Manifestationen bei Epilepsie
Primär betroffen sind Aufmerksamkeit, Gedächtnis, Sprache, Verarbeitungsgeschwindigkeit, Hemmung und Arbeitsgedächtnis. Bei entwicklungsbedingten Enzephalopathien ist die Beeinträchtigung umfassender, sodass interdisziplinäre Teams erforderlich sind.
Die Symptomatik epileptischer Patienten ähnelt oft anderen Neuroentwicklungsstörungen. Daher können Rehabilitationsstrategien aus anderen klinischen Bereichen (kognitive Stimulation, Optimierung oder Kompensation) angewendet werden.
Wichtigster Aspekt in der Intervention ist die Semiotik des Anfalls und seine Entwicklung, da sie kognitives Profil und Verlauf bestimmen.
Epilepsie in anderen Pathologien
Epilepsie tritt auch bei zerebraler Kinderlähmung, genetischen Syndromen, Autismus etc. auf und verschlechtert dort klinische Manifestationen oder verursacht neuropsychologische Regressionen.
Jede wiederkehrende Anfallsform beeinträchtigt kognitive Funktionen, auch als benign geltende kindliche Anfälle. Zwar fehlen initial Symptome, langfristig zeigen sich subtile Defizite (Aufmerksamkeit, Arbeitsgedächtnis, Hemmung). Daher sind auch hier Diagnostik und Monitoring wichtig.
Anforderungen an ein neuropsychologisches Rehabilitationsprogramm bei Epilepsie
Ein neuropsychologisches Rehabilitationsprogramm sollte:
- Auf theoretische Bezugsmodelle zurückgreifen,
- eine interdisziplinäre Perspektive im Umfeld des Kindes (Therapie, Schule, Familie) annehmen,
- Prioritäten klar festlegen,
- Einsatz möglichst früh beginnen,
- ausreichend Therapiedauer (fallabhängig) garantieren,
- auf erhaltene Fähigkeiten aufbauen,
- Emotionale und motivationale Variablen berücksichtigen,
- starke Familienunterstützung einbinden.
Bedeutung der Neurorehabilitation bei Epilepsie
Neurorehabilitation ist nicht nur für kognitive Stimulation und Rehabilita-tion entscheidend, sondern auch, um das kognitive Profil und Anfallsmuster zu verfolgen.
Neuropsychologische Behandlung ermöglicht ein fortlaufendes klinisches Monitoring und schult den Neuropsychologen in der Semiotik einzelner Patienten. So lassen sich subtile klinische Veränderungen oder neue Muster in Anfallsverläufen erkennen, verursacht durch medikamentöse Anpassungen, emotionale Zustände oder Überstimulierung.
Dies erlaubt, kognitive Verschlechterungen oder Krankheitsprogression zu dokumentieren und medikamentöse Anpassungen zu empfehlen, um Nebenwirkungen zu minimieren.
Abschließend sei betont, dass alle Programme (digital oder Papier) lediglich Werkzeuge zur Förderung betroffener Prozesse sind. Erfolg hängt vom definierten Ziel und der Methodik ab.
Kognitive Prozesse sind nicht unabhängig, insbesondere bei netzwerkbasierten Störungen wie Epilepsie. Das menschliche kognitive System beruht auf der Interaktion verschiedener neuropsychologischer Prozesse, die sich in Entwicklung und Erholung gegenseitig beeinflussen. Daher ist es wichtig, keine isolierte Funktionsrehabilitation anzustreben.
Wenn Ihnen dieser Artikel zu Klinischer Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie gefallen hat, könnten Sie auch an folgenden Beiträgen interessiert sein:
Dieser Artikel wurde übersetzt; Link zum Originalartikel auf Spanisch:
Neuropsicología clínica en la neurocirugía de la epilepsia pediátrica
Anfälle, die epileptogene Läsionen verursachen: akute entzündliche Enzephalopathien mit status epilepticus, das Hemiklonus-Hemiplegie-Syndrom (IHHS) oder fieberinduzierte refraktäre Epilepsie-Enzephalopathie (FIRES) unbekannter Ursache.
All diese Störungen beeinträchtigen die normale Gehirnfunktion, führen zu hoher Erregbarkeit und begünstigen je nach Mechanismus verschiedene Anfallsformen.
Klinische Manifestationen nach Anfallstyp
Es ist essenziell, die häufigste Semiotik der verschiedenen Anfallstypen zu erkennen. Dies unterstützt bei der Erstellung eines klinischen Profils, das für Interventions- und Präventionsprogramme unerlässlich ist.
Manchmal sind die klinischen Zeichen sehr subtil. Daher empfiehlt es sich, Familien eine detaillierte Beschreibung der Episoden zu erbitten und, wenn möglich, Videoaufnahmen anzufertigen. Abhängig von der Anfallslokalisation variieren die klinischen Erscheinungen.
Nachfolgend einige häufige klinische Manifestationen bei pädiatrischen Patienten.
1. Temporale fokale Anfälle
Mesiale Temporalanfälle
Patienten können aufsteigendes epigastrisches Unbehagen (brennendes Gefühl im Magen), vermehrtes oder neues Sabbern, Aufstoßen, Blässe, Gesichtsrötung, Atemstillstand, Pupillenerweiterung, Angst, Panik sowie olfaktorische oder gustatorische Halluzinationen zeigen.
Neocorticale Temporalanfälle
Am häufigsten Automatismen (Lutschen, Kauen, Schlucken, Grimassieren, einseitig stärkeres Lächeln) und scheinbares Temporallockern (Blickabwesenheit). Währenddessen ist der Patient amnestisch, wirkt jedoch bewusst, wenn auch verwirrt. Die mittlere Dauer beträgt 1–2 Minuten. Furcht- und Fremdheitsgefühle sind ebenfalls häufig (Etchepareborda, 1999).
2. Frontale fokale Anfälle
Dorsolaterale Region
- Entladungen im vorderen dorsolateralen Frontalbereich: führen zu generalisierten tonisch-klonischen Anfällen mit rascher Ausbreitung, anomalen Augenbewegungen und Bewusstseinsverlust, da sich die Aktivität schnell posterior ausbreitet.
- Entladungen in der dorsolateralen Mitteregion: führen zu komplex-fokalen Anfällen.
- Entladungen unmittelbar vor der Rolando-Furche im neuronalem Kortex: verursachen motorische Symptome, die somatotop der Region folgen (z. B. Finger beginnen zu zucken und breiten sich aus) – so genannte Jackson-Anfälle, meist ohne Bewusstseinsstörung.
- Entladungen im operculären Frontalbereich: führen zu Kau- und Schluckautomatismen, vermehrter Speichelbildung, Dysarthrie und partiellen motorischen Gesichtssymptomen, ohne Bewusstseinsverlust.
Mediale Region
- Entladungen im supplementär-motorischen Bereich: meist Kopf- und Augenrotation zur Gegenseite, gleichzeitig Rumpfrotation in dieselbe Richtung, tonische Kontraktionen des kontralateralen Arms und Dysarthrie (Palacios & Clavijo-Prado, 2016).
- Entladungen in der cingulären oder parakallosalen Region: bimanuale und bipedale Bewegungen, kurze Absencen, unmotiviertes Lachen oder Weinen, Angst- oder Wutanfälle und autonome Zeichen (Tachykardie, Tachypnoe, Pupillenerweiterung) (Etchepareborda, 1999).
Basale Region
- Entladungen in der basalen oder orbitalen Frontalregion: führen zu gestischen Automatismen, tonischen und klonischen Bewegungen aller vier Extremitäten, olfaktorischen Halluzinationen, autonomen Zeichen (Tachykardie, Tachypnoe, Mydriasis) und plötzlichen Stürzen (Etchepareborda, 1999).
3. Absenzen
Eine Form der generalisierten Epilepsie. Typische Absenzen sind plötzliches Einsetzen und Enden bei kurzer Dauer, teils mit oralen oder okulären Bewegungen. Atypische Absenzen verlaufen gradueller und länger, Patienten erinnern sich meist nicht an den Vorfall.
In einigen Absenzformen wirken Patienten bewusst und können sogar sprechen. Manche Absenzen treten bei bestimmten Aktivitäten wie Lesen oder Schreiben auf (Alonso, 2020).
Diese Anfälle beeinträchtigen kognitive Leistungen, besonders bei hoher Frequenz: Patienten kehren verwirrt zurück, was Lernprozesse im familiären und schulischen Umfeld stört. Oft werden sie fälschlich als ADHS oder Lernstörung diagnostiziert.
4. Infantile epileptische Spasmen
Eine seltene Anfallsform. Ohne rechtzeitige Behandlung kann die Neuroentwicklung stagnieren oder regressiv verlaufen.
Charakteristisch sind Spasmen mit Kopfabfall, Hebung und Streckung der Arme und Beine, Rückbogen, Vorbeugen der Rumpfes und Knieflexion im Liegen. Subtile Formen zeigen leichte Kopfabsenkungen oder Augenabweichungen.
Wichtig ist, sie nicht mit Säuglingskoliken, übersteigertem Moro-Reflex oder benignen Schlafmyoklonien zu verwechseln (Alonso, 2020).
Dies sind einige klinische Erscheinungen epileptischer Anfälle. Es gibt zahlreiche weitere, die sich in Ausprägung und Häufigkeit unterscheiden. Bei Neugeborenen und Säuglingen sind Anfälle manchmal subtil oder ähneln nicht-epileptischen paroxysmalen Ereignissen. Bei Zweifeln muss immer eine epileptiforme Pathologie ausgeschlossen werden.
Epilepsiesyndrome mit kognitiven Beeinträchtigungen
Nachfolgend eine kurze Übersicht einiger Enzephalopathie-Syndrome.
1. West-Syndrom
Epileptische Enzephalopathie mit infantilen Spasmen, Hypsarrhythmie (EEG-Muster) und Entwicklungsstillstand in allen Bereichen. Neuropsychologische Profile variieren: von geringer bis starker Beeinträchtigung. Symptomatische Fälle (bekannte Ursache) haben schlechtere Prognose als idiopathische (West-Syndrom-Stiftung, 2011).
2. Lennox-Gastaut-Syndrom
Charakteristische tonische Anfälle v. a. im Schlaf, atonische Anfälle, atypische Absencen und fortschreitender neuropsychologischer Abbau. Später Beginn und günstige Anamnese korrelieren mit besserer Behandlung und kognitivem Outcome. Oft therapieresistent, erfordert Polytherapie, was kognitive Beeinträchtigungen verschlechtert (West-Syndrom-Stiftung, 2011).
3. Dravet-Syndrom
Ein seltenes epileptisches Syndrom, gekennzeichnet durch drei Entwicklungsphasen.
Epidemiologie der Epilepsie und Physiologie des entwickelnden Gehirns
Die Epidemiologie der Epilepsie zeigt eine U-förmige Kurve (siehe Grafik „Epidemiologie der Epilepsie“), mit Spitzen in den ersten zehn Lebensjahren und einem späteren Anstieg im höheren Alter.
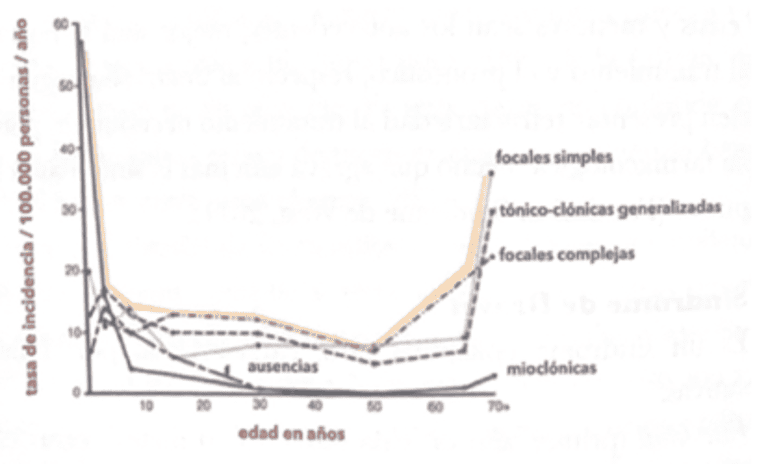
Die Inzidenz kindlicher Epilepsie ist in jüngeren Altersgruppen am höchsten. Epilepsie beeinträchtigt nicht nur die Hirnentwicklung und adaptive Verhaltensweisen, sondern Kinder mit neurologischer Entwicklungsstörung haben ein deutlich erhöhtes Epilepsierisiko. Die Überlappung von Epilepsiesyndromen mit Entwicklungsstörungen ist häufig.
Epileptische Enzephalopathien treten im Frühalter auf, charakterisiert durch EEG-Entladungen, die therapieresistent sind und fortschreitende neurologische Dysfunktionen mit dauerhaften Defiziten in Motorik, Kognition und sozialem Verhalten – typisch für Neuroentwicklungsstörungen.
Andere Entwicklungsstörungen (Rett-Syndrom, Fragiles X, Trisomie 21, Tuberöse Sklerose etc.) bergen hohes Epilepsierisiko, was die Grunderkrankung verschlechtert.
Die höhere Epilepsieneigung in den Lebensextremen hängt wahrscheinlich mit Entwicklungs- bzw. Degenerationsprozessen zusammen: Verbindungen bilden sich im Wachstum und lösen sich im Alter.
Obwohl die synaptischen Mechanismen in beiden Lebensphasen ähnlich gestört sind, sind die Folgen nicht identisch.
Epilepsie im Kindesalter ist häufiger, mit vielfältigen Typen und Syndromen, deren Pathophysiologie eng an die Gehirnentwicklung gekoppelt ist.
Der Entwicklungszeitpunkt beeinflusst Anatomie und Physiologie des Gehirns und damit die Merkmale epileptischer Anfälle.
Betrachtet man die Inzidenz einzelner Anfallsarten (Abb. 4.1), erkennt man:
- Myoklonische Anfälle sind im Neugeborenenalter am häufigsten, da primär motorische und sensorische Areale kaum myelinisiert sind und sich Entladungen nicht ausbreiten. Zwar seltener, aber ebenfalls möglich sind fokale Anfälle.
- Hemikörperliche oder generalisierte Anfälle entwickeln sich erst mit fortschreitender intracorticaler Vernetzung und Myelinisierung.
Die Vernetzung erfolgt postero-anterior in folgenden Regionen:
- Perisylvischer Bereich – ab Geburt,
- Parieto-okzipital – bis 3–7 Monate,
- Prämotorisch-frontal – von 12 Monaten bis ins erste Jahrzehnt.
Parallel verläuft die Myelinisierung kaudal-rostral.
Dies prägt die Semiotik neonataler und infantiler Anfälle, zusätzlich beeinflusst durch hemisphärische Spezialisierung und Entwicklung langer Bahnen.
Für Wachstum, Schaltungsaufbau und -modifikation müssen kindliche Neuronen leicht erregbar sein: GABA wirkt exzitatorisch und Glutamatrezeptoren sind reichlich vorhanden.
Im ersten Lebensjahr dominieren Synaptogenese und Vernetzungsprozesse: Etwa 1000 neue Synapsen pro Sekunde bilden sich, feuern und synchronisieren sich.
Reizübertragung im unreifen Gehirn ist vorrangig exzitatorisch: GABA-Rezeptoren fördern Chlorid-Einstrom und es gibt viele Glutamatrezeptoren. Formende neuronale Schaltkreise haben höhere intrinsische Leitfähigkeit und feuern periodisch, was neue Netze synchronisiert. Dieses exzitatorische Milieu begünstigt Wachstum und Lernen, aber auch epileptische Mechanismen.
Schutzfaktoren gegen Hypererregbarkeit
Intrinsische Schutzfaktoren
Obwohl das kindliche Gehirn hypererregbar ist, tritt Epilepsie nur bei 1–2 % der Unter-Zweijährigen auf, da es über Schutzmechanismen verfügt:
- Hohe Konzentrationen neurotropher Faktoren, die neuroprotektiv wirken,
- Glutamatrezyptor-Reuptake-Transporter in Astrozyten,
- Unreife zytotoxische Schutzmechanismen gegen Glutamattoxizität,
- Geringere Konzentration proinflammatorischer Zytokine.
Extrinsische Schutzfaktoren
Weitere äußere Faktoren tragen bei:
- Oxitocin der Mutter bei Geburt fördert Chlorid-Ausstrom aus fetalen Neuronen und macht GABA inhibitorischer,
- fetales fettreiches Ernährung fördert Ketonkörperbildung mit neuroprotektiver Wirkung.
Ab dem zweiten Lebensjahr verlangsamt sich die Synapsenbildung, die Myelinisierung ist weiter fortgeschritten, wodurch die Epilepsie-Inzidenz sinkt.
Frühe Epilepsie entsteht, wenn schädigende Mechanismen (genetische Defekte, neuronale Migrationsstörungen, entzündliche, infektiöse, traumatische oder tumoröse Ursachen) auf die physiologische Hypererregbarkeit des kindlichen Gehirns einwirken. Sie können an prä- und postsynaptischer Ebene, in der Glia oder an Zelladhäsionsmolekülen wirken und komplex miteinander interagieren.
Störungen synaptischer Proteine führen zu Dysfunktionen neuronaler Schaltkreise und spielen in ätiologischen/lesionalen Mechanismen pädiatrischer Epilepsiesyndrome sowie in Autismus- und Intelligenzminderungs-Erkrankungen eine Rolle.
Genetische Untersuchungen bei kindlicher Epilepsie
Genetische Studien haben Gene aufgedeckt, deren Funktionsverlust neuroentwicklungsstörende Effekte mit oder ohne Epilepsie verursacht.
Beispiel ist das SCN2A-Gen, das die alpha-2-Untereinheit des Natriumkanals codiert. Mutationen können zu variabler Schwere führen:
- Familiäre benign infantile Anfälle (klingen bis zum 2. Lebensjahr ab, ohne Langzeitfolgen),
- Epileptische Enzephalopathie im Säuglingsalter (schwer kontrollierbare Anfälle <1 Jahr, gefolgt von Entwicklungsverzögerung),
- Autismus-Spektrum-Störung, wobei ca. 30 % später Epilepsie entwickeln (nach dem 12. Monat).
Diese genetisch bedingten Epilepsien führten dazu, dass die ILAE 2017 den Begriff „epileptische Enzephalopathie“ auf „Entwicklungs- und epileptische Enzephalopathie“ erweiterte, um Epilepsie uneingeschränkt als Entwicklungsstörung anzuerkennen.
Dies ist ein weiterer Fortschritt in Richtung Anerkennung kindlicher Epilepsie als Neuroentwicklungsstörung, unterstützt von immer mehr Forschungsergebnissen.
Neuropsychologische Diagnostik und Rolle des klinischen Neuropsychologen bei pädiatrischer Epilepsie
Heute gewinnt nicht nur die neuropsychologische Diagnostik von Epilepsiepatienten zunehmend an Bedeutung, sondern auch die Rolle des Neuropsychologen in Epilepsieteams für Diagnostik, chirurgische Intervention und Rehabilitation.
Bei Kindern liefert die neuropsychologische Untersuchung wesentliche Informationen zur Betreuung und Anleitung. Epilepsie kann im sich entwickelnden Gehirn Dysfunktionen in weitreichenden Netzwerken festigen (Fournier, 2019).
Die Ziele der Diagnostik sind diagnostischer Natur: Kognitive oder Verhaltensstörungen liefern wichtige Hinweise zur Lokalisation und Lateralisation der Anfälle, was für die Epilepsiechirurgie sehr hilfreich ist. Zudem unterstützt sie ein besseres Verständnis des Epilepsiesyndroms und damit fundiertere therapeutische Entscheidungen, pharmacologisch und non-pharmacologisch.
Ziele einer neuropsychologischen Untersuchung bei pädiatrischer Epilepsie
Nach Chulune (2010) lassen sich folgende Ziele hervorheben:
- Erfassung eines neuropsychologischen Basisprofils, um Risiken für Entwicklungs-, kognitive, schulische oder psychopathologische Probleme ab dem ersten Anfall zu erkennen.
- Erleichterung der Erkennung neurologischer Störungen, die bei Kindern oft unbemerkt bleiben und als normale Entwicklungsverzögerung fehlgedeutet werden.
- Monitoring kognitiver und Verhaltensänderungen im Krankheitsverlauf.
- Diagnose psychopathologischer Auffälligkeiten und Bewertung ihrer Auswirkung auf Kognition und adaptive Fähigkeiten.
- Unterstützung bei Therapie- und Förderungsplänen und schulischer Maßnahmen.
- Dokumentation möglicher unerwünschter Nebenwirkungen antiepileptischer Medikamente auf kognitiver und verhaltensbezogener Ebene.
Die ILAE empfiehlt, die neuropsychologische Diagnostik als Teil der Routineversorgung von Epilepsiepatienten zu integrieren (Wilson et al., 2015). Der klinische Neuropsychologe sollte weit über Testadministration und statistische Auswertung hinaus aktiv sein, mit umfassender Ausbildung und langjähriger Erfahrung in klinischer und entwicklungsbezogener Neuropsychologie.
Die Analyse der kognitiven Semiotik gewinnt an Bedeutung, um Informationen aus Testverfahren mit der Krankengeschichte und Untersuchung des Patienten zu synthetisieren.
Angesichts der Schwierigkeiten, strukturierte Protokolle bei jungen Kindern mit ausgeprägten Entwicklungsstörungen anzuwenden, ist Anpassungsfähigkeit des Neuropsychologen gefragt, um ein belastbares kognitives Profil zu erstellen.
Neuropsychologische Testprotokolle
Wegen der speziellen Epilepsiefolgen in der Kindheit sind Standardprotokolle, wie bei Erwachsenen, schwer anzuwenden. Internationale und nationale Leitlinien für Kinder existieren kaum.
Wichtig ist, dass man keine noch in Entwicklung befindlichen Funktionen testet. Faktoren wie Aufmerksamkeit, Müdigkeit oder emotionsbedingte Einflüsse sind bei Kindern stärker ausgeprägt. Daher empfiehlt sich Flexibilität, Einführung des Kindes beim Untersucher und Zeitneutralität.
Screening-Tests alleine reichen nicht aus; das Protokoll muss breit genug sein, um verschiedene kognitive Domänen abzudecken. Funktionen wie Gedächtnis sind unter 5 Jahren oft nicht zuverlässig zu prüfen.
Bei exekutiven Funktionen sind verfügbare Tests hoch sensitiv, aber weniger spezifisch, da Sedierung und verlangsamte Informationsverarbeitung durch Antiepileptika viele Ergebnisse sekundär beeinflussen. Somit gewinnen kognitive Semiotik und qualitative Analysen an Bedeutung.
Klinische Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie
Epilepsiechirurgie bei Kindern wird oft nicht als Hauptbehandlungsoption gesehen, sollte aber nicht nur als letzter Schritt bei pharmakoresistenten Fällen betrachtet werden.
Angesichts der Bedeutung des sich entwickelnden Gehirns ist das Hauptziel aller Epilepsiechirurgieteams, die neuroentwicklungsprognose nicht zu verschlechtern. Hierbei ist der Beitrag der Neuropsychologie entscheidend. Der Neuropsychologe ist aktiv bei Auswahl, Evaluation, intraoperativer Betreuung und vor allem postoperativer Anleitung von Familie und Reha-Teams.
Dank fortgeschrittener struktureller und funktioneller Bildgebung lassen sich Kandidaten mit refraktären Läsionen besser erkennen (Berg et al., 2017).
Hauptziele einer neuropsychologischen Untersuchung bei Epilepsiechirurgie
Nach ILAE-Protokoll (Jayakar et al., 2014) sind die Ziele:
- Erstellung einer Basislinie, um Operationsauswirkungen quantitativ zu erfassen,
- Charakterisierung kognitiver Stärken und Defizite, teils vorher unentdeckt,
- Unterstützung bei Lokalisation oder Lateralisation kognitiver Funktionen,
- Information über Risiken postoperativer Defizite,
- Planung von Bildungs- und Rehabilitationsmaßnahmen für Kinder.
Standardpräoperatives Protokoll
- Strukturelles Hochauflösungs-Bildgebungsstudium (3 Tesla MRT),
- Neurophysiologisches Studium mit Video-EEG-Monitoring,
- Komplette neuropsychologische Untersuchung.
Für bestmögliche postoperative Ergebnisse (vollständige Läsionsresektion bei minimalen Funktionseinschränkungen) ist eine exakte Lokalisierung der epileptogenen Zone unerlässlich.
Weshalb es wichtig ist, zwischen symptomatischer Zone (Kortexregion, die durch Entladung Iktalzeichen erzeugt) und irritativer Zone (Region, die interiktale Entladungen generiert und durch EEG/MRT lokalisiert wird) zu unterscheiden.
Entladungen allein erzeugen selten Symptome; meist sind post-entladungsstarke Wellen durch Propagation verantwortlich. Nur selten, wenn Anfälle in eloquenter Zone entstehen, zeigen sich Symptome (Rosenow & Lüders, 2001).
Eine vollständige Läsionsentfernung ist nicht immer nötig und trotz kompletter Resektion können Anfälle persistieren (López & Pomposo-Graztela, 2001). Studien liefern meist nur einen Überblick über Läsionen („Eisbergspitze“), sodass viele finale Resektionsentscheidungen intraoperativ mit direkter Läsionsinformation getroffen werden. Deshalb ist die Präsenz des Neuropsychologen im OP, auch ohne waches Aufwachen, notwendig.
Im pädiatrischen Bereich ist die Rolle des Neuropsychologen noch wichtiger, da er Vertrauen zum Kind aufbaut und die Familie unterstützt.
Hirnplastizität
Die Plastizität im Kindesalter ist entscheidend für die Operationsplanung, nicht nur wegen kognitiver Reorganisation, sondern auch wegen der chronischen Anfallsfolgen in der Neuroentwicklung.
Der neurokognitive Verlauf nach Operation hängt von vielen Faktoren ab:
- Ätiologie der Läsion,
- Alter bei Anfallsbeginn,
- Alter zur OP,
- Interventionsart und Komplikationen,
- medikamentöse Therapie,
- interventionelles Umfeld,
- Zugang zu vorangegangener Neurorehabilitation,
- usw.
Bessere Anfallskontrolle oder Reduktion antiepileptischer Medikamente führt zu deutlicher neurokognitiver Verbesserung.
Die verfügbare Evidenz stammt meist aus Einzelfällen oder kurzen Fallserien. Es bedarf weiterer Dokumentation der neuropsychologischen Entwicklung zur besseren Abwägung von Risiken und Nutzen früher radikaler Eingriffe (Fournier, 2019).
Spezifische Protokolle ähneln den oben genannten, mit Vertiefung in Sprache, Gedächtnis oder visuell-räumliche Funktionen oder Ergänzung psychopatologischer Skalen.
Nachsorge
In der chirurgischen Nachsorge ist es wichtig, das Bewusstsein und grundlegende Funktionen des Kindes beim Aufwachen, in den folgenden Tagen und sechs Monate postoperativ umfassend neuropsychologisch zu bewerten. Ziel ist, Rehabilitations- und Bildungsprogramme festzulegen.
In einigen Fällen (meist 7–8 Jahre) und je nach Läsionslage in eloquenter Zone kann ein intraoperatives Mapping mit wachem Patienten erwogen werden. Hier muss der Neuropsychologe den Patienten im Vorfeld an Tests und Abläufe gewöhnen.
Meist versucht man jedoch, wache intraoperative Protokolle bei Kindern zu vermeiden und greift auf funktionelle MRT oder Wada-Test zurück.
Wenn keine klaren Daten vorliegen oder das Risiko in eloquenter Zone (Sprache, Gedächtnis) hoch ist, ist ein intraoperatives Hirnmapping notwendig. Wann möglich, sollte Monate vor der OP ein longitudinales neuropsychologisches Protokoll erfolgen, um:
- den Patienten longitudinal zu evaluieren,
- Vertrauen zum Kind und der Familie aufzubauen,
- Testtrainings für das intraoperative Mapping durchzuführen.
In dieser Zeit empfiehlt sich ein Programm zur neuropsychologischen Rehabilitation und Stimulation, um bessere prächirurgische, intraoperative Abläufe und eine Reduktion ängstlicher Krisen und posttraumatischer Belastungsreaktionen zu erreichen.
Kognitive Neurorehabilitation bei Epilepsie
Patientenfaktoren für Neurorehabilitationsprogramme
Das neuropsychologische Profil epileptischer Patienten variiert. Für Neurorehabilitation sind folgende Faktoren entscheidend:
1. Alter beim Anfallsbeginn
Das strukturelle und funktionelle Reifealter des Gehirns bestimmt klinische und neurophysiologische Ausdrucksformen. Früher Beginn erhöht Risiko kognitiver Beeinträchtigungen. Studien zeigen, dass das Alter 0–5 Jahre am kritischsten ist (Mauri et al., 2001).
2. Anfallstypen
Generalisierte Anfälle führen normalerweise zu stärkeren kognitiven Beeinträchtigungen als fokale Anfälle.
- Generalisierte Anfälle betreffen tiefe subcorticale Strukturen, Thalamus und retikuläres Formatio-System, die komplexe Funktionen steuern.
- Fokale Epilepsien sind oft mit spezifischen neuropsychologischen Defiziten je nach Anfallslokalisation verbunden (Mulas et al., 2006).
3. Anfallsfrequenz
Häufigere Anfälle beeinträchtigen kognitive Funktionen stärker.
4. Ätiologie oder Epilepsiesyndrom
Epileptische Enzephalopathien (z. B. West, Lennox-Gastaut) haben schlechteste Prognose mit progredienter Beeinträchtigung durch exzessive, diffuse elektrische Aktivität (Nieto, 2011).
5. Pharmakotherapie
Antiepileptika können durch Anfallskontrolle positive kognitive und emotionale Effekte haben, doch sie beeinflussen auch neuronale Netze, die Kognition regulieren, und können unerwünschte neuropsychologische Effekte verursachen.
Moderne Antiepileptika haben geringeren kognitiven Impact, doch zeigt sich in der Praxis weiter eine Beziehung zwischen Medikation und kognitiver Leistung. Beeinträchtigungen sind meist spezifisch und nicht generalisiert.
Monotherapie
Bei zu hohen Blutspiegeln oder rascher Dosissteigerung (Álvarez-Carriles et al., 2011) können auch zwei Medikamente mit geringem kognitiven Nebeneffekt kombinierte Probleme verursachen (Moog, 2009).
Die meisten Antiepileptika reduzieren Membranerregbarkeit, erhöhen postsynaptische Hemmung oder stören Netzsynchronisation. Dies verringert Verarbeitungs- und Aufmerksamkeitsgeschwindigkeit, was in sich entwickelnden Gehirnen stark einschränkend wirken kann.
Allgemeine Nebenwirkungen antiepileptischer Medikamente
Trotz individueller Unterschiede lassen sich folgende Nebenwirkungen festhalten:
- Aufmerksamkeits- und Hemmungsstörungen, verstärkt durch Sedierung oder Schlaflosigkeit,
- Verlangsamung der Informationsverarbeitung,
- Reizbarkeit,
- motorische Unruhe,
- emotionale Dysregulation,
- Beeinträchtigung des Arbeitsgedächtnisses,
- Visusveränderungen,
- usw. (Campos-Castelló & Campos-Soler, 2004).
Größere Defizite finden sich bei pharmakoresistenten Patienten, besonders mit frühem Erkrankungsbeginn, da sie langjährige Chronizität und mehrere Therapien erleben.
Dosis und Anstiegsraten müssen beachtet werden, da kognitive Symptome dosisabhängig zunehmen.
6. Hirnplastizität
Die funktionelle Reorganisation in pädiatrischer Epilepsie zeigt, dass Sprache und Gedächtnis flexibel sind und sich während der Entwicklung verlagern können – etwa von der linken Dominanzregion ins rechte Hemisphären-Pendant oder zu nichttraditionellen Regionen (Brazdil et al., 2005). Dennoch ist dies individuell sehr komplex und erfordert spezialisierte neuropsychologische Rehabilitation.
Diese Faktoren unterscheiden sich je Patient. In Epilepsie sind subkortikale Funktionen (Aufrechterhaltung der Aufmerksamkeit, Arbeitsgedächtnis, Verarbeitungsgeschwindigkeit, kategoriales Abrufen) primär betroffen und verschlechtern sich durch Medikamente zusätzlich.
Klinische und neuropsychologische Manifestationen bei Epilepsie
Primär betroffen sind Aufmerksamkeit, Gedächtnis, Sprache, Verarbeitungsgeschwindigkeit, Hemmung und Arbeitsgedächtnis. Bei entwicklungsbedingten Enzephalopathien ist die Beeinträchtigung umfassender, sodass interdisziplinäre Teams erforderlich sind.
Die Symptomatik epileptischer Patienten ähnelt oft anderen Neuroentwicklungsstörungen. Daher können Rehabilitationsstrategien aus anderen klinischen Bereichen (kognitive Stimulation, Optimierung oder Kompensation) angewendet werden.
Wichtigster Aspekt in der Intervention ist die Semiotik des Anfalls und seine Entwicklung, da sie kognitives Profil und Verlauf bestimmen.
Epilepsie in anderen Pathologien
Epilepsie tritt auch bei zerebraler Kinderlähmung, genetischen Syndromen, Autismus etc. auf und verschlechtert dort klinische Manifestationen oder verursacht neuropsychologische Regressionen.
Jede wiederkehrende Anfallsform beeinträchtigt kognitive Funktionen, auch als benign geltende kindliche Anfälle. Zwar fehlen initial Symptome, langfristig zeigen sich subtile Defizite (Aufmerksamkeit, Arbeitsgedächtnis, Hemmung). Daher sind auch hier Diagnostik und Monitoring wichtig.
Anforderungen an ein neuropsychologisches Rehabilitationsprogramm bei Epilepsie
Ein neuropsychologisches Rehabilitationsprogramm sollte:
- Auf theoretische Bezugsmodelle zurückgreifen,
- eine interdisziplinäre Perspektive im Umfeld des Kindes (Therapie, Schule, Familie) annehmen,
- Prioritäten klar festlegen,
- Einsatz möglichst früh beginnen,
- ausreichend Therapiedauer (fallabhängig) garantieren,
- auf erhaltene Fähigkeiten aufbauen,
- Emotionale und motivationale Variablen berücksichtigen,
- starke Familienunterstützung einbinden.
Bedeutung der Neurorehabilitation bei Epilepsie
Neurorehabilitation ist nicht nur für kognitive Stimulation und Rehabilita-tion entscheidend, sondern auch, um das kognitive Profil und Anfallsmuster zu verfolgen.
Neuropsychologische Behandlung ermöglicht ein fortlaufendes klinisches Monitoring und schult den Neuropsychologen in der Semiotik einzelner Patienten. So lassen sich subtile klinische Veränderungen oder neue Muster in Anfallsverläufen erkennen, verursacht durch medikamentöse Anpassungen, emotionale Zustände oder Überstimulierung.
Dies erlaubt, kognitive Verschlechterungen oder Krankheitsprogression zu dokumentieren und medikamentöse Anpassungen zu empfehlen, um Nebenwirkungen zu minimieren.
Abschließend sei betont, dass alle Programme (digital oder Papier) lediglich Werkzeuge zur Förderung betroffener Prozesse sind. Erfolg hängt vom definierten Ziel und der Methodik ab.
Kognitive Prozesse sind nicht unabhängig, insbesondere bei netzwerkbasierten Störungen wie Epilepsie. Das menschliche kognitive System beruht auf der Interaktion verschiedener neuropsychologischer Prozesse, die sich in Entwicklung und Erholung gegenseitig beeinflussen. Daher ist es wichtig, keine isolierte Funktionsrehabilitation anzustreben.
Wenn Ihnen dieser Artikel zu Klinischer Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie gefallen hat, könnten Sie auch an folgenden Beiträgen interessiert sein:
Dieser Artikel wurde übersetzt; Link zum Originalartikel auf Spanisch:
Neuropsicología clínica en la neurocirugía de la epilepsia pediátrica
Anlässlich des Internationalen Tages der Epilepsie spricht uns der Psychologiestudent Cristian Francisco Liebanas Vega in diesem Artikel über die Klinische Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie. Konkret erklärt er, was Epilepsie ist, die Typen und Ursachen der Epilepsie, die Phasen eines epileptischen Anfalls und die Epilepsiesyndrome, die mit kognitiven Beeinträchtigungen einhergehen. Außerdem betont Liebanas die Bedeutung der neuropsychologischen Diagnostik und der Neurorehabilitation bei Epilepsiepatienten.
Definition und klinische Überlegungen zur Epilepsie
Epilepsie ist, ähnlich wie andere Störungen der neurokognitiven Entwicklung, keine einzelne pathologische Entität. Zwar sind wiederkehrende Anfälle charakteristisch, doch bei einem erheblichen Teil der Kinder und Jugendlichen ist Epilepsie mit intellektuellen, kognitiven und Verhaltensproblemen verbunden.
Anfall, Epilepsie und Epilepsiesyndrom
Gemeinsames Merkmal der Epilepsie sind die Anfälle. Nach der Internationalen Liga gegen Epilepsie (ILAE) definiert sich ein Anfall als „vorübergehendes Auftreten von Zeichen oder Symptomen aufgrund übermäßiger oder synchroner neuronaler Aktivität im Gehirn“.
Arten epileptischer Anfälle
Man unterscheidet zwei grundlegende Formen epileptischer Anfälle:
1. Fokale Anfälle
Lokalisierte Erregbarkeit corticalen oder subcorticalen Ursprungs, die innerhalb auf einen Hemisphärenbereich begrenzter Netzwerke auftritt und stärker lokalisiert oder verteilt sein kann.
Manifestationsformen
Bei dieser Anfallsform kann das Bewusstsein erhalten bleiben oder beeinträchtigt sein. Es lassen sich verschiedene Manifestationsformen beobachten:
- Beginn mit motorischen Zeichen: mit motorischen Automatismen. Es lassen sich verschiedene Anfallstypen unterscheiden, z. B.:
- Atonische Anfälle,
- klonische Anfälle,
- hyperkinetische Anfälle,
- myoklonische Anfälle,
- tonische Anfälle,
- nicht-motorischer Beginn (automatisch).
- Automatische Funktionsstörungen wie Schwitzen, Temperaturveränderungen, vermehrter Speichelfluss etc.
- Sensible Phänomene: Kribbeln, Wärme- oder Kältegefühl, intensive Gerüche, visuelle Störungen oder Schmerzen.
- Kognitive Beeinträchtigungen: Störungen der Sprache oder spezifischer kognitiver Funktionen (Aphasie, Apraxie oder Neglect).
- Gedächtnislücken, Déjà-vu-Gefühle, repetitive Gedanken, Halluzinationen u. a.
- Emotionale Reaktionen: intensive, unangemessene Affekte, Angst, Aggressivität, Weinen, abruptes Lachen oder Weinen.
2. Generalisierte Anfälle
Über den gesamten Kortex verteilt. Sie entstehen in Netzwerken, die bilateral verteilt sind und sich rasch ausbreiten. Diese können corticale und subcorticale Strukturen umfassen und asymmetrisch sein (Berg et al., 2017).
Man unterscheidet:
- Motorische Anfälle: tonisch-klonisch, myoklonisch, myoklonisch-tonisch, myoklonisch-atónisch,
- Nicht-motorische Anfälle (Absencen): typisch oder atypisch, myoklonische Absencen oder mit Lidzuckungen.
Hält ein Anfall länger als 60 Minuten an und spricht nicht auf Medikamente an, spricht man von einem refraktären status epilepticus. Laut ILAE (2017) kann dies langfristige Folgen haben, inklusive neuronaler Schäden oder Tod sowie Störungen neuronaler Netze – abhängig von Anfallstyp und -dauer.
Nicht alle Anfälle sind epileptisch. Es gibt zahlreiche Umstände, die nicht-epileptische Anfälle auslösen können. So wichtig es ist, epileptische Semiotik zu erkennen, ebenso wichtig ist es, nicht-epileptische paroxysmale Störungen zu unterscheiden. Diese resultieren aus Mechanismen, die sich von epileptischen Anfällen unterscheiden, z. B.:
- Anoxische Anfälle (Todesschreianfälle),
- hypnische Anfälle (Nachtschreck),
- psychogene Anfälle (Panikattacken),
- stereotype Bewegungen,
- pathologische Muskelkontraktionen,
- Muskelspasmen,
- etc.
Epilepsie definiert sich als eine dauerhafte Neigung zu epileptischen Anfällen mit neurobiologischen, kognitiven, psychologischen und sozialen Auswirkungen.
Epilepsie liegt vor, wenn mindestens ein unprovozierter Anfall aufgetreten ist und die Wahrscheinlichkeit für einen weiteren Anfall hoch ist. Die ILAE hat daher 2014 eine klinisch-praktische Definition vorgeschlagen, die weiterhin Anwendung findet.
Was ist Epilepsie? Kriterien zur Epilepsiedefinition
- Mindestens zwei unprovozierte Anfälle (oder reflektorische) mit mehr als 24 Stunden Abstand;
- Ein unprovozierter Anfall (oder reflektorisch) und eine Wahrscheinlichkeit für weitere Anfälle in den nächsten zehn Jahren, ähnlich dem allgemeinen Rezidivrisiko (mindestens 60 %) nach zwei unprovozierten Anfällen;
- Diagnose eines Epilepsiesyndroms.
Phasen eines epileptischen Anfalls
Jedes epileptische Ereignis durchläuft meist drei Phasen: Prä-Anfall, Anfallsbeginn und Post-Anfall.
1. Prä-Anfall-Phase
In dieser Phase wirken auslösende oder prädisponierende Faktoren wie Fieber, Überstimulation oder Schlafmangel. Man sollte bei jedem Patienten erkennen, welche Reize Anfälle begünstigen, um sie möglichst zu meiden oder zu reduzieren.
Manchmal sind Umweltreize Auslöser, z. B. Lichtblitze oder unerwartete Geräusche. Bei schweren Epilepsie-Enzephalopathien kann sogar sensorische Stimulation Anfälle triggern. Bei motorisch betroffenen Enzephalopathien treten Anfälle oft beim Versuch willkürlicher Bewegungen auf.
2. Anfallsbeginn
Hier treten die klinischen Zeichen des jeweiligen Anfallstyps auf. Am auffälligsten sind generalisierte tonisch-klonische Anfälle, es gibt aber auch subtilere Formen wie myoklonische Lidzuckungen.
3. Post-Anfall-Phase
Die postiktale Phase zeigt u. a. Kopfschmerzen, Schläfrigkeit, Muskelschwäche.
Ein Epilepsiesyndrom ist definiert als ein Charakteristikum klinischer Befunde und EEG-Muster, oft mit spezifischen ätiologischen Befunden (strukturell, genetisch, metabolisch, immunologisch oder infektiös). Es hat prognostische und therapeutische Implikationen und zeigt häufig altersabhängige Präsentationen.
Viele Syndrome sind mit bestimmten komorbiden intellektuellen, psychiatrischen und anderen Störungen verbunden, während in anderen Syndromen das Fehlen solcher Komorbiditäten charakteristisch ist.
Epilepsiesyndrome nach Alter des Auftretens
Traditionell werden Epilepsiesyndrome nach dem Alter geordnet. Die ILAE unterscheidet:
- Neonatale und Säuglingssyndrome (bis 2 Jahre),
- Kindheitssyndrome,
- Syndrome mit variabler Altersmanifestation (pediatrisch und erwachsen).
Tritt Epilepsie auf, während das nervöse System sich entwickelt, zeigen sich typische neurologische Defizite im Kindesalter, die als Störungen der Neuroentwicklung gelten.
Es gibt epidemiologische, anatomische, physiopathologische und entwicklungsbezogene Gründe, Epilepsie bei Kindern und Jugendlichen als Neuroentwicklungsstörung zu betrachten: Das unreife Gehirn ist hypererregbar, Eigenschaften ändern sich im Reifeprozess und führen zu altersabhängigen Epilepsiesyndromen (Mas Salguero, 2020).
Ursachen der Epilepsie
Seit 2017 empfiehlt die ILAE, Epilepsie nach Ursache und Komorbiditäten, z. B. Neuroentwicklungsstörungen, zu klassifizieren, um Anfallskontrolle und Lebensqualität zu verbessern. Bei Kindern und Jugendlichen lassen sich drei Hauptgruppen unterscheiden:
1. Symptomatische Epilepsie
Verursacht durch jegliche Schädigung des Gehirns: Frühgeburtsfolgen, Infektionen, Malformationen, Traumata, Hypoxie etc.
2. Genetisch bedingte Epilepsie
Meist durch De-novo-Mutationen (z. B. Dravet-Syndrom), teils erblich (z. B. familiäre neonatale benigne Anfälle).
Anfälle, die epileptogene Läsionen verursachen: akute entzündliche Enzephalopathien mit status epilepticus, das Hemiklonus-Hemiplegie-Syndrom (IHHS) oder fieberinduzierte refraktäre Epilepsie-Enzephalopathie (FIRES) unbekannter Ursache.
All diese Störungen beeinträchtigen die normale Gehirnfunktion, führen zu hoher Erregbarkeit und begünstigen je nach Mechanismus verschiedene Anfallsformen.
Klinische Manifestationen nach Anfallstyp
Es ist essenziell, die häufigste Semiotik der verschiedenen Anfallstypen zu erkennen. Dies unterstützt bei der Erstellung eines klinischen Profils, das für Interventions- und Präventionsprogramme unerlässlich ist.
Manchmal sind die klinischen Zeichen sehr subtil. Daher empfiehlt es sich, Familien eine detaillierte Beschreibung der Episoden zu erbitten und, wenn möglich, Videoaufnahmen anzufertigen. Abhängig von der Anfallslokalisation variieren die klinischen Erscheinungen.
Nachfolgend einige häufige klinische Manifestationen bei pädiatrischen Patienten.
1. Temporale fokale Anfälle
Mesiale Temporalanfälle
Patienten können aufsteigendes epigastrisches Unbehagen (brennendes Gefühl im Magen), vermehrtes oder neues Sabbern, Aufstoßen, Blässe, Gesichtsrötung, Atemstillstand, Pupillenerweiterung, Angst, Panik sowie olfaktorische oder gustatorische Halluzinationen zeigen.
Neocorticale Temporalanfälle
Am häufigsten Automatismen (Lutschen, Kauen, Schlucken, Grimassieren, einseitig stärkeres Lächeln) und scheinbares Temporallockern (Blickabwesenheit). Währenddessen ist der Patient amnestisch, wirkt jedoch bewusst, wenn auch verwirrt. Die mittlere Dauer beträgt 1–2 Minuten. Furcht- und Fremdheitsgefühle sind ebenfalls häufig (Etchepareborda, 1999).
2. Frontale fokale Anfälle
Dorsolaterale Region
- Entladungen im vorderen dorsolateralen Frontalbereich: führen zu generalisierten tonisch-klonischen Anfällen mit rascher Ausbreitung, anomalen Augenbewegungen und Bewusstseinsverlust, da sich die Aktivität schnell posterior ausbreitet.
- Entladungen in der dorsolateralen Mitteregion: führen zu komplex-fokalen Anfällen.
- Entladungen unmittelbar vor der Rolando-Furche im neuronalem Kortex: verursachen motorische Symptome, die somatotop der Region folgen (z. B. Finger beginnen zu zucken und breiten sich aus) – so genannte Jackson-Anfälle, meist ohne Bewusstseinsstörung.
- Entladungen im operculären Frontalbereich: führen zu Kau- und Schluckautomatismen, vermehrter Speichelbildung, Dysarthrie und partiellen motorischen Gesichtssymptomen, ohne Bewusstseinsverlust.
Mediale Region
- Entladungen im supplementär-motorischen Bereich: meist Kopf- und Augenrotation zur Gegenseite, gleichzeitig Rumpfrotation in dieselbe Richtung, tonische Kontraktionen des kontralateralen Arms und Dysarthrie (Palacios & Clavijo-Prado, 2016).
- Entladungen in der cingulären oder parakallosalen Region: bimanuale und bipedale Bewegungen, kurze Absencen, unmotiviertes Lachen oder Weinen, Angst- oder Wutanfälle und autonome Zeichen (Tachykardie, Tachypnoe, Pupillenerweiterung) (Etchepareborda, 1999).
Basale Region
- Entladungen in der basalen oder orbitalen Frontalregion: führen zu gestischen Automatismen, tonischen und klonischen Bewegungen aller vier Extremitäten, olfaktorischen Halluzinationen, autonomen Zeichen (Tachykardie, Tachypnoe, Mydriasis) und plötzlichen Stürzen (Etchepareborda, 1999).
3. Absenzen
Eine Form der generalisierten Epilepsie. Typische Absenzen sind plötzliches Einsetzen und Enden bei kurzer Dauer, teils mit oralen oder okulären Bewegungen. Atypische Absenzen verlaufen gradueller und länger, Patienten erinnern sich meist nicht an den Vorfall.
In einigen Absenzformen wirken Patienten bewusst und können sogar sprechen. Manche Absenzen treten bei bestimmten Aktivitäten wie Lesen oder Schreiben auf (Alonso, 2020).
Diese Anfälle beeinträchtigen kognitive Leistungen, besonders bei hoher Frequenz: Patienten kehren verwirrt zurück, was Lernprozesse im familiären und schulischen Umfeld stört. Oft werden sie fälschlich als ADHS oder Lernstörung diagnostiziert.
4. Infantile epileptische Spasmen
Eine seltene Anfallsform. Ohne rechtzeitige Behandlung kann die Neuroentwicklung stagnieren oder regressiv verlaufen.
Charakteristisch sind Spasmen mit Kopfabfall, Hebung und Streckung der Arme und Beine, Rückbogen, Vorbeugen der Rumpfes und Knieflexion im Liegen. Subtile Formen zeigen leichte Kopfabsenkungen oder Augenabweichungen.
Wichtig ist, sie nicht mit Säuglingskoliken, übersteigertem Moro-Reflex oder benignen Schlafmyoklonien zu verwechseln (Alonso, 2020).
Dies sind einige klinische Erscheinungen epileptischer Anfälle. Es gibt zahlreiche weitere, die sich in Ausprägung und Häufigkeit unterscheiden. Bei Neugeborenen und Säuglingen sind Anfälle manchmal subtil oder ähneln nicht-epileptischen paroxysmalen Ereignissen. Bei Zweifeln muss immer eine epileptiforme Pathologie ausgeschlossen werden.
Epilepsiesyndrome mit kognitiven Beeinträchtigungen
Nachfolgend eine kurze Übersicht einiger Enzephalopathie-Syndrome.
1. West-Syndrom
Epileptische Enzephalopathie mit infantilen Spasmen, Hypsarrhythmie (EEG-Muster) und Entwicklungsstillstand in allen Bereichen. Neuropsychologische Profile variieren: von geringer bis starker Beeinträchtigung. Symptomatische Fälle (bekannte Ursache) haben schlechtere Prognose als idiopathische (West-Syndrom-Stiftung, 2011).
2. Lennox-Gastaut-Syndrom
Charakteristische tonische Anfälle v. a. im Schlaf, atonische Anfälle, atypische Absencen und fortschreitender neuropsychologischer Abbau. Später Beginn und günstige Anamnese korrelieren mit besserer Behandlung und kognitivem Outcome. Oft therapieresistent, erfordert Polytherapie, was kognitive Beeinträchtigungen verschlechtert (West-Syndrom-Stiftung, 2011).
3. Dravet-Syndrom
Ein seltenes epileptisches Syndrom, gekennzeichnet durch drei Entwicklungsphasen.
Epidemiologie der Epilepsie und Physiologie des entwickelnden Gehirns
Die Epidemiologie der Epilepsie zeigt eine U-förmige Kurve (siehe Grafik „Epidemiologie der Epilepsie“), mit Spitzen in den ersten zehn Lebensjahren und einem späteren Anstieg im höheren Alter.

Die Inzidenz kindlicher Epilepsie ist in jüngeren Altersgruppen am höchsten. Epilepsie beeinträchtigt nicht nur die Hirnentwicklung und adaptive Verhaltensweisen, sondern Kinder mit neurologischer Entwicklungsstörung haben ein deutlich erhöhtes Epilepsierisiko. Die Überlappung von Epilepsiesyndromen mit Entwicklungsstörungen ist häufig.
Epileptische Enzephalopathien treten im Frühalter auf, charakterisiert durch EEG-Entladungen, die therapieresistent sind und fortschreitende neurologische Dysfunktionen mit dauerhaften Defiziten in Motorik, Kognition und sozialem Verhalten – typisch für Neuroentwicklungsstörungen.
Andere Entwicklungsstörungen (Rett-Syndrom, Fragiles X, Trisomie 21, Tuberöse Sklerose etc.) bergen hohes Epilepsierisiko, was die Grunderkrankung verschlechtert.
Die höhere Epilepsieneigung in den Lebensextremen hängt wahrscheinlich mit Entwicklungs- bzw. Degenerationsprozessen zusammen: Verbindungen bilden sich im Wachstum und lösen sich im Alter.
Obwohl die synaptischen Mechanismen in beiden Lebensphasen ähnlich gestört sind, sind die Folgen nicht identisch.
Epilepsie im Kindesalter ist häufiger, mit vielfältigen Typen und Syndromen, deren Pathophysiologie eng an die Gehirnentwicklung gekoppelt ist.
Der Entwicklungszeitpunkt beeinflusst Anatomie und Physiologie des Gehirns und damit die Merkmale epileptischer Anfälle.
Betrachtet man die Inzidenz einzelner Anfallsarten (Abb. 4.1), erkennt man:
- Myoklonische Anfälle sind im Neugeborenenalter am häufigsten, da primär motorische und sensorische Areale kaum myelinisiert sind und sich Entladungen nicht ausbreiten. Zwar seltener, aber ebenfalls möglich sind fokale Anfälle.
- Hemikörperliche oder generalisierte Anfälle entwickeln sich erst mit fortschreitender intracorticaler Vernetzung und Myelinisierung.
Die Vernetzung erfolgt postero-anterior in folgenden Regionen:
- Perisylvischer Bereich – ab Geburt,
- Parieto-okzipital – bis 3–7 Monate,
- Prämotorisch-frontal – von 12 Monaten bis ins erste Jahrzehnt.
Parallel verläuft die Myelinisierung kaudal-rostral.
Dies prägt die Semiotik neonataler und infantiler Anfälle, zusätzlich beeinflusst durch hemisphärische Spezialisierung und Entwicklung langer Bahnen.
Für Wachstum, Schaltungsaufbau und -modifikation müssen kindliche Neuronen leicht erregbar sein: GABA wirkt exzitatorisch und Glutamatrezeptoren sind reichlich vorhanden.
Im ersten Lebensjahr dominieren Synaptogenese und Vernetzungsprozesse: Etwa 1000 neue Synapsen pro Sekunde bilden sich, feuern und synchronisieren sich.
Reizübertragung im unreifen Gehirn ist vorrangig exzitatorisch: GABA-Rezeptoren fördern Chlorid-Einstrom und es gibt viele Glutamatrezeptoren. Formende neuronale Schaltkreise haben höhere intrinsische Leitfähigkeit und feuern periodisch, was neue Netze synchronisiert. Dieses exzitatorische Milieu begünstigt Wachstum und Lernen, aber auch epileptische Mechanismen.
Schutzfaktoren gegen Hypererregbarkeit
Intrinsische Schutzfaktoren
Obwohl das kindliche Gehirn hypererregbar ist, tritt Epilepsie nur bei 1–2 % der Unter-Zweijährigen auf, da es über Schutzmechanismen verfügt:
- Hohe Konzentrationen neurotropher Faktoren, die neuroprotektiv wirken,
- Glutamatrezyptor-Reuptake-Transporter in Astrozyten,
- Unreife zytotoxische Schutzmechanismen gegen Glutamattoxizität,
- Geringere Konzentration proinflammatorischer Zytokine.
Extrinsische Schutzfaktoren
Weitere äußere Faktoren tragen bei:
- Oxitocin der Mutter bei Geburt fördert Chlorid-Ausstrom aus fetalen Neuronen und macht GABA inhibitorischer,
- fetales fettreiches Ernährung fördert Ketonkörperbildung mit neuroprotektiver Wirkung.
Ab dem zweiten Lebensjahr verlangsamt sich die Synapsenbildung, die Myelinisierung ist weiter fortgeschritten, wodurch die Epilepsie-Inzidenz sinkt.
Frühe Epilepsie entsteht, wenn schädigende Mechanismen (genetische Defekte, neuronale Migrationsstörungen, entzündliche, infektiöse, traumatische oder tumoröse Ursachen) auf die physiologische Hypererregbarkeit des kindlichen Gehirns einwirken. Sie können an prä- und postsynaptischer Ebene, in der Glia oder an Zelladhäsionsmolekülen wirken und komplex miteinander interagieren.
Störungen synaptischer Proteine führen zu Dysfunktionen neuronaler Schaltkreise und spielen in ätiologischen/lesionalen Mechanismen pädiatrischer Epilepsiesyndrome sowie in Autismus- und Intelligenzminderungs-Erkrankungen eine Rolle.
Genetische Untersuchungen bei kindlicher Epilepsie
Genetische Studien haben Gene aufgedeckt, deren Funktionsverlust neuroentwicklungsstörende Effekte mit oder ohne Epilepsie verursacht.
Beispiel ist das SCN2A-Gen, das die alpha-2-Untereinheit des Natriumkanals codiert. Mutationen können zu variabler Schwere führen:
- Familiäre benign infantile Anfälle (klingen bis zum 2. Lebensjahr ab, ohne Langzeitfolgen),
- Epileptische Enzephalopathie im Säuglingsalter (schwer kontrollierbare Anfälle <1 Jahr, gefolgt von Entwicklungsverzögerung),
- Autismus-Spektrum-Störung, wobei ca. 30 % später Epilepsie entwickeln (nach dem 12. Monat).
Diese genetisch bedingten Epilepsien führten dazu, dass die ILAE 2017 den Begriff „epileptische Enzephalopathie“ auf „Entwicklungs- und epileptische Enzephalopathie“ erweiterte, um Epilepsie uneingeschränkt als Entwicklungsstörung anzuerkennen.
Dies ist ein weiterer Fortschritt in Richtung Anerkennung kindlicher Epilepsie als Neuroentwicklungsstörung, unterstützt von immer mehr Forschungsergebnissen.
Neuropsychologische Diagnostik und Rolle des klinischen Neuropsychologen bei pädiatrischer Epilepsie
Heute gewinnt nicht nur die neuropsychologische Diagnostik von Epilepsiepatienten zunehmend an Bedeutung, sondern auch die Rolle des Neuropsychologen in Epilepsieteams für Diagnostik, chirurgische Intervention und Rehabilitation.
Bei Kindern liefert die neuropsychologische Untersuchung wesentliche Informationen zur Betreuung und Anleitung. Epilepsie kann im sich entwickelnden Gehirn Dysfunktionen in weitreichenden Netzwerken festigen (Fournier, 2019).
Die Ziele der Diagnostik sind diagnostischer Natur: Kognitive oder Verhaltensstörungen liefern wichtige Hinweise zur Lokalisation und Lateralisation der Anfälle, was für die Epilepsiechirurgie sehr hilfreich ist. Zudem unterstützt sie ein besseres Verständnis des Epilepsiesyndroms und damit fundiertere therapeutische Entscheidungen, pharmacologisch und non-pharmacologisch.
Ziele einer neuropsychologischen Untersuchung bei pädiatrischer Epilepsie
Nach Chulune (2010) lassen sich folgende Ziele hervorheben:
- Erfassung eines neuropsychologischen Basisprofils, um Risiken für Entwicklungs-, kognitive, schulische oder psychopathologische Probleme ab dem ersten Anfall zu erkennen.
- Erleichterung der Erkennung neurologischer Störungen, die bei Kindern oft unbemerkt bleiben und als normale Entwicklungsverzögerung fehlgedeutet werden.
- Monitoring kognitiver und Verhaltensänderungen im Krankheitsverlauf.
- Diagnose psychopathologischer Auffälligkeiten und Bewertung ihrer Auswirkung auf Kognition und adaptive Fähigkeiten.
- Unterstützung bei Therapie- und Förderungsplänen und schulischer Maßnahmen.
- Dokumentation möglicher unerwünschter Nebenwirkungen antiepileptischer Medikamente auf kognitiver und verhaltensbezogener Ebene.
Die ILAE empfiehlt, die neuropsychologische Diagnostik als Teil der Routineversorgung von Epilepsiepatienten zu integrieren (Wilson et al., 2015). Der klinische Neuropsychologe sollte weit über Testadministration und statistische Auswertung hinaus aktiv sein, mit umfassender Ausbildung und langjähriger Erfahrung in klinischer und entwicklungsbezogener Neuropsychologie.
Die Analyse der kognitiven Semiotik gewinnt an Bedeutung, um Informationen aus Testverfahren mit der Krankengeschichte und Untersuchung des Patienten zu synthetisieren.
Angesichts der Schwierigkeiten, strukturierte Protokolle bei jungen Kindern mit ausgeprägten Entwicklungsstörungen anzuwenden, ist Anpassungsfähigkeit des Neuropsychologen gefragt, um ein belastbares kognitives Profil zu erstellen.
Neuropsychologische Testprotokolle
Wegen der speziellen Epilepsiefolgen in der Kindheit sind Standardprotokolle, wie bei Erwachsenen, schwer anzuwenden. Internationale und nationale Leitlinien für Kinder existieren kaum.
Wichtig ist, dass man keine noch in Entwicklung befindlichen Funktionen testet. Faktoren wie Aufmerksamkeit, Müdigkeit oder emotionsbedingte Einflüsse sind bei Kindern stärker ausgeprägt. Daher empfiehlt sich Flexibilität, Einführung des Kindes beim Untersucher und Zeitneutralität.
Screening-Tests alleine reichen nicht aus; das Protokoll muss breit genug sein, um verschiedene kognitive Domänen abzudecken. Funktionen wie Gedächtnis sind unter 5 Jahren oft nicht zuverlässig zu prüfen.
Bei exekutiven Funktionen sind verfügbare Tests hoch sensitiv, aber weniger spezifisch, da Sedierung und verlangsamte Informationsverarbeitung durch Antiepileptika viele Ergebnisse sekundär beeinflussen. Somit gewinnen kognitive Semiotik und qualitative Analysen an Bedeutung.
Klinische Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie
Epilepsiechirurgie bei Kindern wird oft nicht als Hauptbehandlungsoption gesehen, sollte aber nicht nur als letzter Schritt bei pharmakoresistenten Fällen betrachtet werden.
Angesichts der Bedeutung des sich entwickelnden Gehirns ist das Hauptziel aller Epilepsiechirurgieteams, die neuroentwicklungsprognose nicht zu verschlechtern. Hierbei ist der Beitrag der Neuropsychologie entscheidend. Der Neuropsychologe ist aktiv bei Auswahl, Evaluation, intraoperativer Betreuung und vor allem postoperativer Anleitung von Familie und Reha-Teams.
Dank fortgeschrittener struktureller und funktioneller Bildgebung lassen sich Kandidaten mit refraktären Läsionen besser erkennen (Berg et al., 2017).
Hauptziele einer neuropsychologischen Untersuchung bei Epilepsiechirurgie
Nach ILAE-Protokoll (Jayakar et al., 2014) sind die Ziele:
- Erstellung einer Basislinie, um Operationsauswirkungen quantitativ zu erfassen,
- Charakterisierung kognitiver Stärken und Defizite, teils vorher unentdeckt,
- Unterstützung bei Lokalisation oder Lateralisation kognitiver Funktionen,
- Information über Risiken postoperativer Defizite,
- Planung von Bildungs- und Rehabilitationsmaßnahmen für Kinder.
Standardpräoperatives Protokoll
- Strukturelles Hochauflösungs-Bildgebungsstudium (3 Tesla MRT),
- Neurophysiologisches Studium mit Video-EEG-Monitoring,
- Komplette neuropsychologische Untersuchung.
Für bestmögliche postoperative Ergebnisse (vollständige Läsionsresektion bei minimalen Funktionseinschränkungen) ist eine exakte Lokalisierung der epileptogenen Zone unerlässlich.
Weshalb es wichtig ist, zwischen symptomatischer Zone (Kortexregion, die durch Entladung Iktalzeichen erzeugt) und irritativer Zone (Region, die interiktale Entladungen generiert und durch EEG/MRT lokalisiert wird) zu unterscheiden.
Entladungen allein erzeugen selten Symptome; meist sind post-entladungsstarke Wellen durch Propagation verantwortlich. Nur selten, wenn Anfälle in eloquenter Zone entstehen, zeigen sich Symptome (Rosenow & Lüders, 2001).
Eine vollständige Läsionsentfernung ist nicht immer nötig und trotz kompletter Resektion können Anfälle persistieren (López & Pomposo-Graztela, 2001). Studien liefern meist nur einen Überblick über Läsionen („Eisbergspitze“), sodass viele finale Resektionsentscheidungen intraoperativ mit direkter Läsionsinformation getroffen werden. Deshalb ist die Präsenz des Neuropsychologen im OP, auch ohne waches Aufwachen, notwendig.
Im pädiatrischen Bereich ist die Rolle des Neuropsychologen noch wichtiger, da er Vertrauen zum Kind aufbaut und die Familie unterstützt.
Hirnplastizität
Die Plastizität im Kindesalter ist entscheidend für die Operationsplanung, nicht nur wegen kognitiver Reorganisation, sondern auch wegen der chronischen Anfallsfolgen in der Neuroentwicklung.
Der neurokognitive Verlauf nach Operation hängt von vielen Faktoren ab:
- Ätiologie der Läsion,
- Alter bei Anfallsbeginn,
- Alter zur OP,
- Interventionsart und Komplikationen,
- medikamentöse Therapie,
- interventionelles Umfeld,
- Zugang zu vorangegangener Neurorehabilitation,
- usw.
Bessere Anfallskontrolle oder Reduktion antiepileptischer Medikamente führt zu deutlicher neurokognitiver Verbesserung.
Die verfügbare Evidenz stammt meist aus Einzelfällen oder kurzen Fallserien. Es bedarf weiterer Dokumentation der neuropsychologischen Entwicklung zur besseren Abwägung von Risiken und Nutzen früher radikaler Eingriffe (Fournier, 2019).
Spezifische Protokolle ähneln den oben genannten, mit Vertiefung in Sprache, Gedächtnis oder visuell-räumliche Funktionen oder Ergänzung psychopatologischer Skalen.
Nachsorge
In der chirurgischen Nachsorge ist es wichtig, das Bewusstsein und grundlegende Funktionen des Kindes beim Aufwachen, in den folgenden Tagen und sechs Monate postoperativ umfassend neuropsychologisch zu bewerten. Ziel ist, Rehabilitations- und Bildungsprogramme festzulegen.
In einigen Fällen (meist 7–8 Jahre) und je nach Läsionslage in eloquenter Zone kann ein intraoperatives Mapping mit wachem Patienten erwogen werden. Hier muss der Neuropsychologe den Patienten im Vorfeld an Tests und Abläufe gewöhnen.
Meist versucht man jedoch, wache intraoperative Protokolle bei Kindern zu vermeiden und greift auf funktionelle MRT oder Wada-Test zurück.
Wenn keine klaren Daten vorliegen oder das Risiko in eloquenter Zone (Sprache, Gedächtnis) hoch ist, ist ein intraoperatives Hirnmapping notwendig. Wann möglich, sollte Monate vor der OP ein longitudinales neuropsychologisches Protokoll erfolgen, um:
- den Patienten longitudinal zu evaluieren,
- Vertrauen zum Kind und der Familie aufzubauen,
- Testtrainings für das intraoperative Mapping durchzuführen.
In dieser Zeit empfiehlt sich ein Programm zur neuropsychologischen Rehabilitation und Stimulation, um bessere prächirurgische, intraoperative Abläufe und eine Reduktion ängstlicher Krisen und posttraumatischer Belastungsreaktionen zu erreichen.
Kognitive Neurorehabilitation bei Epilepsie
Patientenfaktoren für Neurorehabilitationsprogramme
Das neuropsychologische Profil epileptischer Patienten variiert. Für Neurorehabilitation sind folgende Faktoren entscheidend:
1. Alter beim Anfallsbeginn
Das strukturelle und funktionelle Reifealter des Gehirns bestimmt klinische und neurophysiologische Ausdrucksformen. Früher Beginn erhöht Risiko kognitiver Beeinträchtigungen. Studien zeigen, dass das Alter 0–5 Jahre am kritischsten ist (Mauri et al., 2001).
2. Anfallstypen
Generalisierte Anfälle führen normalerweise zu stärkeren kognitiven Beeinträchtigungen als fokale Anfälle.
- Generalisierte Anfälle betreffen tiefe subcorticale Strukturen, Thalamus und retikuläres Formatio-System, die komplexe Funktionen steuern.
- Fokale Epilepsien sind oft mit spezifischen neuropsychologischen Defiziten je nach Anfallslokalisation verbunden (Mulas et al., 2006).
3. Anfallsfrequenz
Häufigere Anfälle beeinträchtigen kognitive Funktionen stärker.
4. Ätiologie oder Epilepsiesyndrom
Epileptische Enzephalopathien (z. B. West, Lennox-Gastaut) haben schlechteste Prognose mit progredienter Beeinträchtigung durch exzessive, diffuse elektrische Aktivität (Nieto, 2011).
5. Pharmakotherapie
Antiepileptika können durch Anfallskontrolle positive kognitive und emotionale Effekte haben, doch sie beeinflussen auch neuronale Netze, die Kognition regulieren, und können unerwünschte neuropsychologische Effekte verursachen.
Moderne Antiepileptika haben geringeren kognitiven Impact, doch zeigt sich in der Praxis weiter eine Beziehung zwischen Medikation und kognitiver Leistung. Beeinträchtigungen sind meist spezifisch und nicht generalisiert.
Monotherapie
Bei zu hohen Blutspiegeln oder rascher Dosissteigerung (Álvarez-Carriles et al., 2011) können auch zwei Medikamente mit geringem kognitiven Nebeneffekt kombinierte Probleme verursachen (Moog, 2009).
Die meisten Antiepileptika reduzieren Membranerregbarkeit, erhöhen postsynaptische Hemmung oder stören Netzsynchronisation. Dies verringert Verarbeitungs- und Aufmerksamkeitsgeschwindigkeit, was in sich entwickelnden Gehirnen stark einschränkend wirken kann.
Allgemeine Nebenwirkungen antiepileptischer Medikamente
Trotz individueller Unterschiede lassen sich folgende Nebenwirkungen festhalten:
- Aufmerksamkeits- und Hemmungsstörungen, verstärkt durch Sedierung oder Schlaflosigkeit,
- Verlangsamung der Informationsverarbeitung,
- Reizbarkeit,
- motorische Unruhe,
- emotionale Dysregulation,
- Beeinträchtigung des Arbeitsgedächtnisses,
- Visusveränderungen,
- usw. (Campos-Castelló & Campos-Soler, 2004).
Größere Defizite finden sich bei pharmakoresistenten Patienten, besonders mit frühem Erkrankungsbeginn, da sie langjährige Chronizität und mehrere Therapien erleben.
Dosis und Anstiegsraten müssen beachtet werden, da kognitive Symptome dosisabhängig zunehmen.
6. Hirnplastizität
Die funktionelle Reorganisation in pädiatrischer Epilepsie zeigt, dass Sprache und Gedächtnis flexibel sind und sich während der Entwicklung verlagern können – etwa von der linken Dominanzregion ins rechte Hemisphären-Pendant oder zu nichttraditionellen Regionen (Brazdil et al., 2005). Dennoch ist dies individuell sehr komplex und erfordert spezialisierte neuropsychologische Rehabilitation.
Diese Faktoren unterscheiden sich je Patient. In Epilepsie sind subkortikale Funktionen (Aufrechterhaltung der Aufmerksamkeit, Arbeitsgedächtnis, Verarbeitungsgeschwindigkeit, kategoriales Abrufen) primär betroffen und verschlechtern sich durch Medikamente zusätzlich.
Klinische und neuropsychologische Manifestationen bei Epilepsie
Primär betroffen sind Aufmerksamkeit, Gedächtnis, Sprache, Verarbeitungsgeschwindigkeit, Hemmung und Arbeitsgedächtnis. Bei entwicklungsbedingten Enzephalopathien ist die Beeinträchtigung umfassender, sodass interdisziplinäre Teams erforderlich sind.
Die Symptomatik epileptischer Patienten ähnelt oft anderen Neuroentwicklungsstörungen. Daher können Rehabilitationsstrategien aus anderen klinischen Bereichen (kognitive Stimulation, Optimierung oder Kompensation) angewendet werden.
Wichtigster Aspekt in der Intervention ist die Semiotik des Anfalls und seine Entwicklung, da sie kognitives Profil und Verlauf bestimmen.
Epilepsie in anderen Pathologien
Epilepsie tritt auch bei zerebraler Kinderlähmung, genetischen Syndromen, Autismus etc. auf und verschlechtert dort klinische Manifestationen oder verursacht neuropsychologische Regressionen.
Jede wiederkehrende Anfallsform beeinträchtigt kognitive Funktionen, auch als benign geltende kindliche Anfälle. Zwar fehlen initial Symptome, langfristig zeigen sich subtile Defizite (Aufmerksamkeit, Arbeitsgedächtnis, Hemmung). Daher sind auch hier Diagnostik und Monitoring wichtig.
Anforderungen an ein neuropsychologisches Rehabilitationsprogramm bei Epilepsie
Ein neuropsychologisches Rehabilitationsprogramm sollte:
- Auf theoretische Bezugsmodelle zurückgreifen,
- eine interdisziplinäre Perspektive im Umfeld des Kindes (Therapie, Schule, Familie) annehmen,
- Prioritäten klar festlegen,
- Einsatz möglichst früh beginnen,
- ausreichend Therapiedauer (fallabhängig) garantieren,
- auf erhaltene Fähigkeiten aufbauen,
- Emotionale und motivationale Variablen berücksichtigen,
- starke Familienunterstützung einbinden.
Bedeutung der Neurorehabilitation bei Epilepsie
Neurorehabilitation ist nicht nur für kognitive Stimulation und Rehabilita-tion entscheidend, sondern auch, um das kognitive Profil und Anfallsmuster zu verfolgen.
Neuropsychologische Behandlung ermöglicht ein fortlaufendes klinisches Monitoring und schult den Neuropsychologen in der Semiotik einzelner Patienten. So lassen sich subtile klinische Veränderungen oder neue Muster in Anfallsverläufen erkennen, verursacht durch medikamentöse Anpassungen, emotionale Zustände oder Überstimulierung.
Dies erlaubt, kognitive Verschlechterungen oder Krankheitsprogression zu dokumentieren und medikamentöse Anpassungen zu empfehlen, um Nebenwirkungen zu minimieren.
Abschließend sei betont, dass alle Programme (digital oder Papier) lediglich Werkzeuge zur Förderung betroffener Prozesse sind. Erfolg hängt vom definierten Ziel und der Methodik ab.
Kognitive Prozesse sind nicht unabhängig, insbesondere bei netzwerkbasierten Störungen wie Epilepsie. Das menschliche kognitive System beruht auf der Interaktion verschiedener neuropsychologischer Prozesse, die sich in Entwicklung und Erholung gegenseitig beeinflussen. Daher ist es wichtig, keine isolierte Funktionsrehabilitation anzustreben.
Wenn Ihnen dieser Artikel zu Klinischer Neuropsychologie in der Neurochirurgie bei pädiatrischer Epilepsie gefallen hat, könnten Sie auch an folgenden Beiträgen interessiert sein:
Dieser Artikel wurde übersetzt; Link zum Originalartikel auf Spanisch:
Neuropsicología clínica en la neurocirugía de la epilepsia pediátrica






 Arbeitsblatt zur Förderung der räumlichen Orientierung mit Kindern: Räume das Haus auf
Arbeitsblatt zur Förderung der räumlichen Orientierung mit Kindern: Räume das Haus auf
Schreiben Sie einen Kommentar