Аспирантка Марта Арбису Гомес представляет недавнее исследование «Фосфо‑tau217 в плазме для диагностики болезни Альцгеймера в первичной и вторичной медпомощи с использованием полностью автоматизированной платформы», в котором изложена точность и надежность анализа плазменного p‑tau217 для диагностики болезни Альцгеймера.
Почему нам нужен кровяной биомаркер для болезни Альцгеймера?
Больница болезнь Альцгеймера (БА) представляет собой одну из крупнейших медицинских проблем XXI века, поскольку затрагивает миллионы людей и создает растущее бремя для систем здравоохранения и семей.
Традиционно установленный диагноз БА основывается на инвазивных методах (люмбальная пункция для анализа ликвора) или дорогостоящих исследованиях (ПЭТ головного мозга для визуализации амилоида и тау). Эти процедуры, помимо того что неудобны и не всегда доступны, как правило, оставляют подтверждение диагноза на более поздние стадии заболевания, когда нейрональное повреждение уже значительно.
В связи с этим наличие надежного, быстрого и автоматизируемого кровяного биомаркера позволило бы:
- Обнаруживать патологические изменения на доклинических или очень ранних стадиях, открывая возможность для ранних вмешательств.
- Облегчить скрининг в первичной помощи, разгружая неврологические консультации и сокращая время ожидания.
- Снизить затраты и логистические барьеры, применяя обычные лабораторные платформы без необходимости специализированного оборудования.
Исследование, опубликованное 9 апреля 2025 года в Nature Medicine, как раз направлено на решение этой потребности, впервые в крупномасштабном исследовании оценивая потенциал фосфо‑tau217 (p‑tau217) в плазме, измеренного с помощью полностью автоматизированного иммуноанализа.
Как проводилось исследование по оценке анализа плазменного p-tau217 для диагностики болезни Альцгеймера?
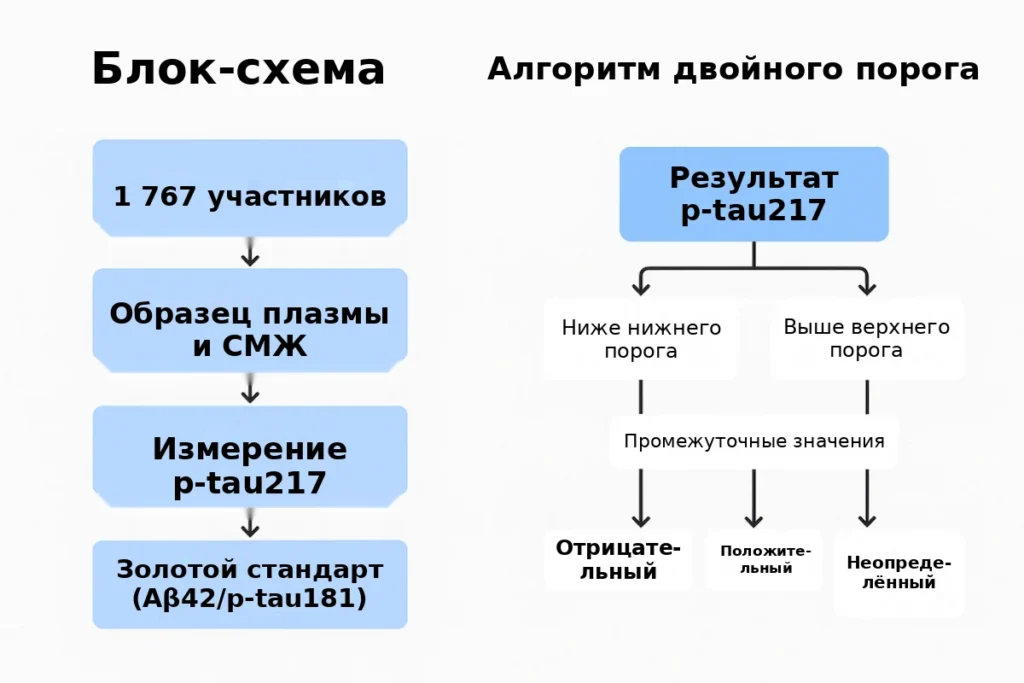
Для обеспечения строгого и репрезентативного подхода исследователи собрали 1 767 участников с легкими когнитивными нарушениями или ранней деменцией, участники были из центров первичной и вторичной медицинской помощи в Швеции, Испании и Италии. Такое географическое и организационное разнообразие важно для понимания работы биомаркера в различных клинических условиях.
В качестве «золотого стандарта» для подтверждения наличия патологии Альцгеймера использовали анализ ликвора с измерением классических маркеров амилоид‑β42 и p‑tau181. Таким образом каждая плазменная проба могла быть напрямую сопоставлена с установленным диагнозом. Следует отметить, что количественное определение p‑tau217 в плазме выполнялось на платформе Lumipulse™ компании Fujirebio — полностью автоматизированной системе, которая снижает человеческую вариабельность и позволяет обрабатывать большие объемы образцов с высокой воспроизводимостью.
Такая надежная схема гарантирует, что результаты отражают как точность иммуноанализа, так и его практическую применимость в рутинных лабораториях.
Каковы ключевые результаты по биомаркеру p-tau217 в диагностике болезни Альцгеймера?
Основные выводы показывают, что анализ p‑tau217 в плазме достигает диагностической точности 89–91% в условиях вторичной помощи (неврология и нейропсихология) и 85% в первичной помощи (врачи общей практики). Эти данные подтверждают, что даже без доступа к сложной визуализационной технике медицинские центры могут надежно выявлять пациентов с БА.
Прогностические показатели также оказались очень высокими: положительная прогностическая ценность (VPP) варьировала от 82% до 95%, тогда как отрицательная прогностическая ценность (VPN) достигала 77%–90%. На практике это означает, что как ложноположительные, так и ложноотрицательные результаты остаются на низком уровне, что обеспечивает эффективный и безопасный скрининг.
Особенно примечательна устойчивость биомаркера: его эффективность не зависела от клинических переменных, таких как пожилой возраст (у пациентов ≥ 80 лет точность составляла 83%), наличие хронических коморбидностей, пол или генотип APOE. Кроме того, при применении стратегии с двойным порогом — с нижней и верхней границей — точность удалось повысить до 92–94%, при этом от 12% до 17% образцов оставались неклассифицированными с промежуточными значениями для минимизации неопределенных диагнозов.
| Показатель | Значение |
|---|---|
| Точность во вторичной помощи | 89% – 91% |
| Точность в первичной помощи | 85% |
| Положительная прогностическая ценность (VPP) | 82% – 95% |
| Отрицательная прогностическая ценность (VPN) | 77% – 90% |
| Точность у участников ≥ 80 лет | 83% |
| Точность при двойном пороге | 92% – 94% |
| Неопределенные образцы (промежуточный порог) | 12% – 17% |
Какие последствия для клинической практики имеет этот анализ p-tau217?
Эти результаты меняют подход к диагностике болезни Альцгеймера по нескольким направлениям:
- Ранний скрининг в первичной помощи: возможность для врача общей практики назначить анализ p‑tau217 и получить надежный результат экономит лишние направления к специалистам и ускоряет диагностический процесс. Таким образом пациент быстрее попадает на специализированный прием, когда вмешательство наиболее эффективно.
- Мониторинг и наблюдение: легко повторяемый кровяной биомаркер упрощает оценку ответа на фармакологическое лечение или когнитивные вмешательства, а также мониторинг прогрессирования заболевания во времени без использования инвазивных процедур.
- Стандартизация и масштабируемость: автоматизация на платформе Lumipulse™ обеспечивает сопоставимые результаты между лабораториями и регионами, что способствует многоцентровому сотрудничеству и внедрению единых протоколов в системах здравоохранения.
В сумме эти преимущества указывают на модель интегрированной помощи, где биологическое выявление болезни Альцгеймера сочетается с программами когнитивной реабилитации и цифровым наблюдением, предлагая пациенту целостный подход.
Как это достижение связано с NeuronUP?
В NeuronUP разрабатываются инструменты когнитивной реабилитации, основанные на научных данных. Включение биологических биомаркеров, таких как p‑tau217, дополняет цифровые инструменты, позволяя:
- Персонализировать программы в зависимости от реальной патологической нагрузки у пациента.
- Измерять влияние вмешательств не только клинически, но и на биологическом уровне.
- Сотрудничать с лабораториями и медицинскими центрами для оказания мультидисциплинарной помощи, объединяющей раннюю диагностику и когнитивную стимуляцию.
Это исследование укрепляет концепцию комплексного лечения болезни: пока биомедицинские достижения улучшают выявление, NeuronUP оптимизирует функциональное восстановление и качество жизни.
Заключение
Анализ плазменного p‑tau217, валидированный в этом крупном многоцентровом исследовании, предоставляет быстрый, надежный и доступный инструмент для диагностики болезни Альцгеймера. Его применение в первичной и вторичной медпомощи, а также потенциал для мониторинга открывают новые возможности для ранней и персонализированной помощи. В контексте NeuronUP эти выводы стимулируют тесное сотрудничество между биологической диагностикой и когнитивными терапиями, продвигая более комплексный и эффективный уход.
Библиография
- Palmqvist S, Warmenhoven N, Anastasi F, Pilotto A, Janelidze S, Tideman P, Stomrud E, Mattsson‑Carlgren N, Smith R, Ossenkoppele R, Tan K, Dittrich A, Skoog I, Zetterberg H, Quaresima V, Tolassi C, Höglund K, Brugnoni D, Puig‑Pijoan A, Fernández‑Lebrero A, Contador J, Padovani A, Monane M, Verghese PB, Braunstein JB, Kern S, Blennow K, Ashton NJ, Suárez‑Calvet M, Hansson O. Plasma phospho‑tau217 for Alzheimer’s disease diagnosis in primary and secondary care using a fully automated platform. Nature Medicine. 2025 Apr 9. doi:10.1038/s41591-025-03622-w.
Если вам понравилась эта запись блога о точности и надежности анализа плазменного p‑tau217 для диагностики болезни Альцгеймера, вам наверняка будут интересны эти статьи NeuronUP:
«Эта статья была переведена. Ссылка на оригинальную статью на испанском:»
Precisión y fiabilidad de la prueba de plasma p-tau217 para el diagnóstico de la enfermedad de Alzheimer







Добавить комментарий