A doutoranda Marta Arbizu Gómez aborda uma questão importante: os modelos de idade cerebral (BrainAge) refletem as alterações específicas do Alzheimer ou capturam o envelhecimento normal do cérebro?
Resumo executivo:
BrainAge é um biomarcador que estima a idade cerebral, mas nem sempre distingue entre envelhecimento normal e Alzheimer. Os estudos mostram que a neuroimagem prediz melhor a idade cerebral, enquanto os testes neuropsicológicos são mais eficazes para diagnosticar a doença. Na Espanha, combinar ambos permite melhorar a avaliação clínica e a reabilitação cognitiva com ferramentas como NeuronUP.
O que é a idade cerebral e por que interessa no Alzheimer?
O envelhecimento é o principal fator de risco para a doença de Alzheimer (EA), mas envelhecimento e neurodegeneração não são exatamente a mesma coisa. À medida que as pessoas envelhecem, o cérebro experimenta mudanças estruturais e funcionais naturais. Contudo, no Alzheimer essas mudanças aceleram-se e afetam regiões cerebrais-chave implicadas na memória e na cognição.
Nos últimos anos, os investigadores desenvolveram modelos de idade cerebral (BrainAge), algoritmos de aprendizado de máquina capazes de estimar a idade biológica do cérebro a partir de dados de neuroimagem ou testes cognitivos. A ideia é simples: se o cérebro de uma pessoa parece “mais velho” do que a sua idade cronológica indica, isso pode ser um sinal precoce de declínio neurológico.
A diferença entre a idade cerebral estimada e a idade cronológica é denominada BrainAge Delta. Um valor positivo indica que o cérebro parece mais envelhecido do que o esperado, enquanto um valor negativo sugere um cérebro mais “jovem”.
No entanto, surge uma questão importante: esses modelos realmente refletem as alterações específicas do Alzheimer ou simplesmente capturam o envelhecimento normal do cérebro? Um estudo recente publicado em NeuroImage, e liderado pelo Laboratório de Neuroimagem Computacional do Instituto de Pesquisa em Saúde Biobizkaia, aborda precisamente essa questão, analisando como as variáveis usadas nos modelos BrainAge influenciam a capacidade de identificar a doença de Alzheimer.

Inscreva-se
na nossa
Newsletter
Como foi conduzida esta investigação sobre idade cerebral e Alzheimer?
Para responder a essa pergunta, os investigadores usaram dados do projeto Alzheimer’s Disease Neuroimaging Initiative (ADNI), uma das bases de dados internacionais mais utilizadas na investigação sobre demências.
O estudo incluiu participantes pertencentes a cinco grupos clínicos:
- Pessoas cognitivamente saudáveis (CN).
- Pessoas com comprometimento cognitivo leve (MCI).
- Pacientes com doença de Alzheimer (AD).
- MCI estável (sMCI).
- MCI que progride para Alzheimer (pMCI).
Os modelos foram treinados usando dois tipos principais de variáveis:
Dados de neuroimagem
Extraídos de ressonância magnética estrutural (T1):
- volume de matéria cinzenta,
- volume de matéria branca,
- volume do hipocampo,
- amígdala,
- tálamo,
- putâmen,
- núcleo caudado,
- líquido cefalorraquidiano, entre outros.
Essas medidas refletem mudanças estruturais no cérebro associadas tanto ao envelhecimento quanto à neurodegeneração.
Variáveis neuropsicológicas
Também foram incluídas pontuações de testes cognitivos amplamente usados na clínica:
- MMSE,
- ADAS,
- MoCA,
- FAQ,
- pontuação de memória ADNI,
- função executiva ADNI.
Os investigadores analisaram quais variáveis eram mais úteis para dois objetivos distintos:
- Prever a idade cerebral.
- Distinguir entre diferentes grupos clínicos.
Posteriormente treinaram diferentes modelos BrainAge usando combinações progressivas dessas variáveis.
Resultados-chave do estudo sobre idade cerebral e Alzheimer
Os resultados mostram uma diferença clara entre os tipos de variáveis utilizadas.
As variáveis derivadas de ressonância magnética —como o volume de matéria cinzenta ou do hipocampo— foram as mais informativas para prever a idade cerebral. Por outro lado, os testes neuropsicológicos mostraram-se mais eficazes para distinguir entre pessoas saudáveis e pacientes com doença de Alzheimer.
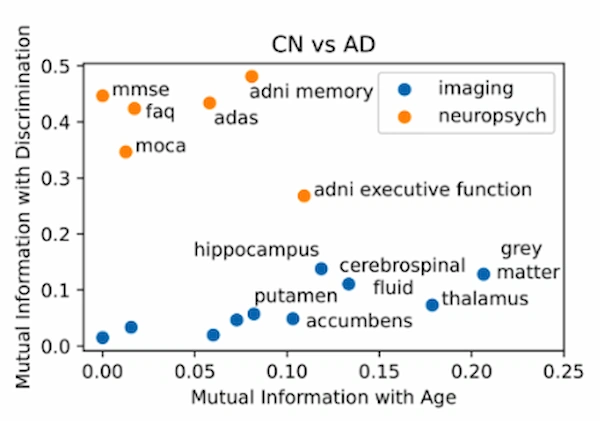
Esse padrão sugere que os modelos que tentam estimar a idade cerebral podem capturar processos de envelhecimento normais que nem sempre refletem a patologia específica do Alzheimer.
Neuroimagem: melhor para estimar a idade
As variáveis derivadas de ressonância magnética —como o volume de matéria cinzenta ou do hipocampo— foram as mais informativas para prever a idade cerebral.
Isto faz sentido, pois o envelhecimento normal produz mudanças estruturais progressivas no cérebro.
Testes cognitivos: melhores para identificar a doença
Por outro lado, os testes neuropsicológicos mostraram-se mais eficazes para distinguir entre pessoas saudáveis, comprometimento cognitivo leve e Alzheimer.
Ou seja, embora as imagens cerebrais capturem bem o envelhecimento, o desempenho cognitivo reflete melhor as diferenças clínicas entre os grupos.
Uma descoberta importante: precisão versus utilidade clínica
Um dos resultados mais interessantes do estudo é que existe um compromisso entre a precisão na previsão da idade e a capacidade de classificar a doença.
Quando os modelos são otimizados usando variáveis mais relacionadas com o envelhecimento, o erro na previsão da idade diminui. No entanto, a sua capacidade de distinguir entre pessoas saudáveis e pacientes com Alzheimer nem sempre melhora. Pelo contrário, quando se priorizam variáveis com maior capacidade discriminativa, a classificação dos grupos clínicos melhora, embora a estimativa da idade cerebral perca precisão.
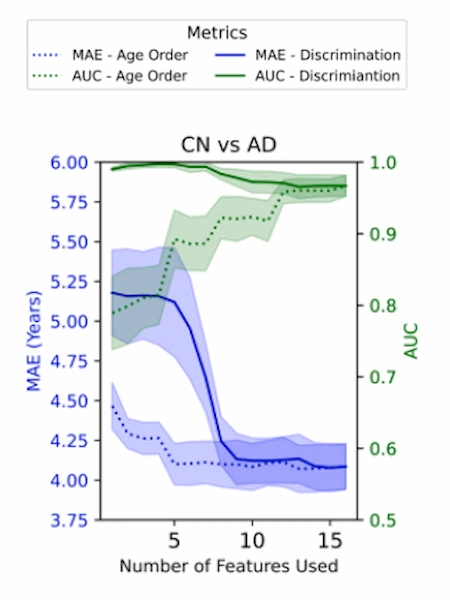
Esse resultado sugere que as mudanças associadas ao envelhecimento e as mudanças associadas ao Alzheimer não são exatamente os mesmos processos biológicos.
O papel-chave do hipocampo
Entre todas as variáveis analisadas, o hipocampo destacou-se como uma das regiões cerebrais mais relevantes.
O seu volume mostrou uma forte capacidade de diferenciar entre os distintos grupos clínicos, o que coincide com a evidência prévia: o hipocampo é uma das primeiras estruturas afetadas pela patologia do Alzheimer e a sua atrofia relaciona-se estreitamente com os déficits de memória.
Os modelos BrainAge são úteis para diagnosticar Alzheimer?
Os investigadores compararam também duas estratégias diferentes:
- Classificar os pacientes utilizando o BrainAge delta.
- Classificá-los utilizando diretamente as variáveis cerebrais.
Os resultados mostraram que, em muitos casos, usar as variáveis diretamente era igual ou até mais eficaz do que utilizar o BrainAge delta.
Isto indica que os modelos BrainAge nem sempre fornecem informação adicional para o diagnóstico.
No entanto, apresentam uma vantagem conceptual importante: geram uma única métrica contínua, que poderia ser utilizada como indicador de risco ou como ferramenta para monitorar a progressão da doença ao longo do tempo.
Quais implicações isso tem para a pesquisa em Alzheimer?
Este estudo traz várias conclusões relevantes para o desenvolvimento de biomarcadores baseados em inteligência artificial:
- Separar envelhecimento e doença é fundamental. Modelos que tentam capturar ambos os processos simultaneamente podem confundir mudanças normais do envelhecimento com neurodegeneração.
- A seleção de variáveis é chave. Dependendo do objetivo —prever a idade ou detectar a doença— devem ser utilizados diferentes tipos de variáveis.
- Os modelos devem ser projetados para tarefas específicas. Um modelo otimizado para estimar a idade biológica não será necessariamente o melhor para diagnosticar Alzheimer.
Em definitiva, o envelhecimento não é simplesmente o “ruído” de fundo na doença de Alzheimer, mas um processo que interage ativamente com a patologia.
Como esse avanço se relaciona com a NeuronUP?
Compreender melhor a diferença entre envelhecimento cerebral e deterioração neurodegenerativa tem implicações diretas para a reabilitação cognitiva.
Em plataformas como NeuronUP, utilizadas para o treino cognitivo e a estimulação de funções executivas, memória ou atenção, dispor de biomarcadores confiáveis pode ajudar a:
- identificar pacientes em fases iniciais.
- personalizar programas de reabilitação de acordo com o perfil cognitivo.
- monitorar a evolução dos pacientes ao longo do tempo.
Enquanto ferramentas como BrainAge contribuem para melhorar a detecção e a compreensão da doença, soluções digitais como NeuronUP permitem intervir no funcionamento cognitivo e na qualidade de vida dos pacientes.
Este estudo foi liderado pelo Dr. Jesus M. Cortes, que também é Diretor de Pesquisa na NeuronUP, desde o Instituto de Investigação Sanitária BioBizkaia e em colaboração com pesquisadores da Harvard Medical School, University Carlos III de Madrid, Vrije Universiteit Amsterdam, Brigham & Women’s, University of Melbourne, Ikerbasque e a Universidad del País Vasco.
Conclusões para profissionais
Os modelos BrainAge representam uma ferramenta promissora para estudar o envelhecimento cerebral e sua relação com a doença de Alzheimer. Contudo, este estudo demonstra que a relação entre idade cerebral e neurodegeneração é complexa.
As variáveis estruturais do cérebro são especialmente úteis para estimar a idade biológica, enquanto os testes cognitivos mostram-se mais eficazes para distinguir entre diferentes estados clínicos.
Por isso, o desenvolvimento de modelos preditivos em Alzheimer deve levar em conta qual processo se quer estudar —envelhecimento ou doença— e selecionar cuidadosamente as variáveis utilizadas.
No futuro, integrar biomarcadores biológicos, neuroimagem e ferramentas digitais de avaliação e reabilitação cognitiva pode oferecer uma visão mais completa e personalizada do tratamento do Alzheimer.
Bibliografia
- Garcia Condado J, Verdugo Recuero I, Tellaetxe-Elorriaga I, Birkenbihl C, Carrigan M, Diez I, Buckley RF, Erramuzpe A, Cortes JM. Aging as an active player in Alzheimer’s disease classification: Insights from feature selection in BrainAge models. NeuroImage. 2025. doi:10.1016/j.neuroimage.2025.121548.
Perguntas frequentes sobre idade cerebral (BrainAge) e Alzheimer
1. O que é o BrainAge Delta e como ajuda a detectar o envelhecimento acelerado?
O BrainAge Delta é a diferença métrica entre a idade biológica do cérebro (estimada por IA) e a idade cronológica do paciente.
- Valor positivo: Indica um cérebro que parece ‘mais velho’ do que o esperado, o que é um sinal de alerta precoce de deterioração neurológica.
- Valor negativo: Sugere um cérebro ‘mais jovem’, o que costuma estar associado a uma melhor reserva cognitiva.
Em centros de neurorreabilitação, essa métrica permite monitorar objetivamente o risco de progressão do paciente.
2. A idade cerebral é suficiente para diagnosticar o Alzheimer na clínica?
Não por si só. Segundo a investigação liderada pelo Instituto de Investigação Sanitária BioBizkaia, existe um ‘trade-off’ entre a precisão ao prever a idade e a capacidade para diagnosticar a doença.
Modelos que melhor estimam a idade nem sempre são os mais eficazes para distinguir entre um cérebro saudável e um com Alzheimer. De fato, usar diretamente as variáveis cerebrais pode ser igual ou mais eficaz do que o cálculo do BrainAge Delta para o diagnóstico clínico.
3. Quais variáveis discriminam melhor a doença de Alzheimer: a neuroimagem ou os testes cognitivos?
O estudo demonstra que a escolha da ferramenta depende do objetivo clínico:
- Neuroimagem (Ressonância Magnética T1): É a mais informativa para prever a idade cerebral e captar o envelhecimento natural.
- Testes Neuropsicológicos (MMSE, MoCA, ADAS): São significativamente mais eficazes para discriminar clinicamente entre pacientes saudáveis, com comprometimento cognitivo leve (CCL) e Alzheimer.
Isto confirma que o desempenho cognitivo reflete melhor as diferenças patológicas do que a estrutura cerebral isolada.
4. Por que o hipocampo é chave nos modelos BrainAge?
O volume do hipocampo destaca-se como uma das regiões mais relevantes pela sua dualidade:
- É fundamental para estimar a idade biológica.
- Possui uma forte capacidade para diferenciar grupos clínicos porque é uma das primeiras estruturas afetadas pela atrofia no Alzheimer.
A sua análise é vital para qualquer programa de estimulação cognitiva centrado na memória.
6. Quais implicações têm estas descobertas para a reabilitação cognitiva?
Compreender a interação entre envelhecimento e patologia permite aos profissionais em Espanha e América Latina desenhar intervenções mais personalizadas. O uso de biomarcadores digitais e modelos de IA ajuda a:
- Identificar fases iniciais: Detectar pacientes antes que o declínio seja evidente.
- Personalizar programas: Ajustar a estimulação de funções executivas e atenção em plataformas como NeuronUP segundo o perfil biológico do usuário.
- Acompanhamento preciso: Avaliar o impacto da reabilitação na “saúde cerebral” ao longo do tempo.
7. Por que é importante separar envelhecimento e doença no Alzheimer?
Porque misturar ambos processos pode levar a interpretações erradas. O estudo demonstra que os modelos BrainAge podem captar o envelhecimento normal, por isso é fundamental selecionar bem as variáveis conforme o objetivo clínico.




 Neuromodulação do sono na neurorehabilitação: Técnicas não invasivas para a estimulação cognitiva
Neuromodulação do sono na neurorehabilitação: Técnicas não invasivas para a estimulação cognitiva
Deixe um comentário