La doctoranda Marta Arbizu Gómez aborda una cuestión importante: ¿reflejan los modelos de edad cerebral (BrainAge) los cambios específicos del alzhéimer o capturan el envejecimiento normal del cerebro?
Resumen ejecutivo:
BrainAge es un biomarcador que estima la edad cerebral, pero no siempre distingue entre envejecimiento normal y alzhéimer. Los estudios muestran que la neuroimagen predice mejor la edad cerebral, mientras que las pruebas neuropsicológicas son más eficaces para diagnosticar la enfermedad. En España, combinar ambas permite mejorar la evaluación clínica y la rehabilitación cognitiva con herramientas como NeuronUP.
¿Qué es la edad cerebral y por qué interesa en el alzhéimer?
El envejecimiento es el principal factor de riesgo para la enfermedad de Alzheimer (EA), pero envejecimiento y neurodegeneración no son exactamente lo mismo. A medida que las personas envejecen, el cerebro experimenta cambios estructurales y funcionales naturales. Sin embargo, en el alzhéimer estos cambios se aceleran y afectan a regiones cerebrales clave implicadas en la memoria y la cognición.
En los últimos años, los investigadores han desarrollado modelos de edad cerebral (BrainAge), algoritmos de aprendizaje automático capaces de estimar la edad biológica del cerebro a partir de datos de neuroimagen o pruebas cognitivas. La idea es sencilla: si el cerebro de una persona parece “más viejo” de lo que indica su edad cronológica, podría ser una señal temprana de deterioro neurológico.
La diferencia entre la edad cerebral estimada y la edad real se denomina BrainAge Delta. Un valor positivo indica que el cerebro parece más envejecido de lo esperado, mientras que un valor negativo sugiere un cerebro más “joven”.
Sin embargo, surge una cuestión importante: ¿reflejan realmente estos modelos los cambios específicos del alhéimer o simplemente capturan el envejecimiento normal del cerebro? Un estudio reciente publicado en NeuroImage, y liderado por el Laboratorio de Neuroimagen Computacional del Instituto de Investigación Sanitaria Biobizkaia, aborda precisamente esta cuestión, analizando cómo influyen las variables utilizadas en los modelos BrainAge en la capacidad para identificar la enfermedad de Alzheimer.
¿Cómo se llevó a cabo esta investigación sobre edad cerebral y alzhéimer?
Para responder a esta pregunta, los investigadores utilizaron datos del proyecto Alzheimer’s Disease Neuroimaging Initiative (ADNI), una de las bases de datos internacionales más utilizadas en investigación sobre demencias.
El estudio incluyó participantes pertenecientes a cinco grupos clínicos:
- Personas cognitivamente sanas (CN).
- Personas con deterioro cognitivo leve (MCI).
- Pacientes con enfermedad de Alzheimer (AD).
- MCI estable (sMCI).
- MCI que progresa a Alzheimer (pMCI).
Los modelos se entrenaron utilizando dos tipos de variables principales:
Datos de neuroimagen
Extraídos de resonancia magnética estructural (T1):
- volumen de materia gris,
- volumen de materia blanca,
- volumen del hipocampo,
- amígdala,
- tálamo,
- putamen,
- caudado,
- líquido cefalorraquídeo, entre otros.
Estas medidas reflejan cambios estructurales en el cerebro asociados tanto al envejecimiento como a la neurodegeneración.
Variables neuropsicológicas
También se incluyeron puntuaciones de pruebas cognitivas ampliamente utilizadas en clínica:
- MMSE,
- ADAS,
- MoCA,
- FAQ,
- puntuación de memoria ADNI,
- función ejecutiva ADNI.
Los investigadores analizaron qué variables eran más útiles para dos objetivos distintos:
- Predecir la edad cerebral.
- Distinguir entre diferentes grupos clínicos.
Posteriormente entrenaron distintos modelos BrainAge utilizando combinaciones progresivas de estas variables.
Resultados clave del estudio sobre edad cerebral y alzhéimer
Los resultados muestran una diferencia clara entre los tipos de variables utilizadas.
Las variables derivadas de resonancia magnética —como el volumen de materia gris o del hipocampo— fueron las más informativas para predecir la edad cerebral. Por el contrario, las pruebas neuropsicológicas resultaron más eficaces para distinguir entre personas sanas y pacientes con enfermedad de Alzheimer.
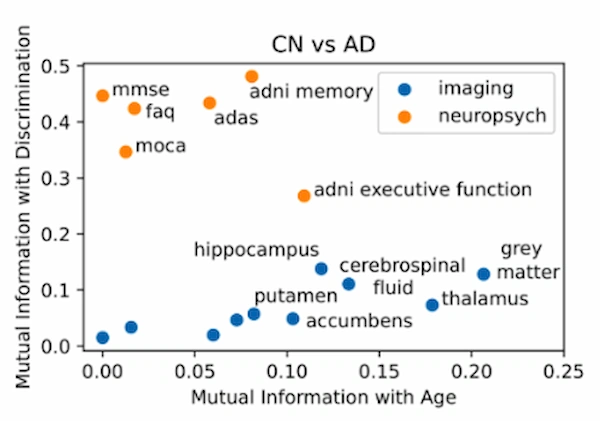
Este patrón sugiere que los modelos que intentan estimar la edad cerebral pueden capturar procesos de envejecimiento normales que no necesariamente reflejan la patología específica del Alzheimer.
Neuroimagen: mejor para estimar la edad
Las variables derivadas de resonancia magnética —como el volumen de materia gris o del hipocampo— fueron las más informativas para predecir la edad cerebral.
Esto tiene sentido, ya que el envejecimiento normal produce cambios estructurales progresivos en el cerebro.
Pruebas cognitivas: mejor para identificar la enfermedad
En cambio, las pruebas neuropsicológicas resultaron más eficaces para distinguir entre personas sanas, deterioro cognitivo leve y alzhéimer.
Es decir, aunque las imágenes cerebrales capturan bien el envejecimiento, el rendimiento cognitivo refleja mejor las diferencias clínicas entre los grupos.
Un hallazgo importante: precisión frente a utilidad clínica
Uno de los resultados más interesantes del estudio es que existe un compromiso entre precisión en la predicción de edad y capacidad para clasificar la enfermedad.
Cuando los modelos se optimizan utilizando variables más relacionadas con el envejecimiento, el error en la predicción de edad disminuye. Sin embargo, su capacidad para distinguir entre personas sanas y pacientes con alzhéimer no siempre mejora. Por el contrario, cuando se priorizan variables con mayor capacidad discriminativa, la clasificación de los grupos clínicos mejora, aunque la estimación de la edad cerebral pierde precisión.
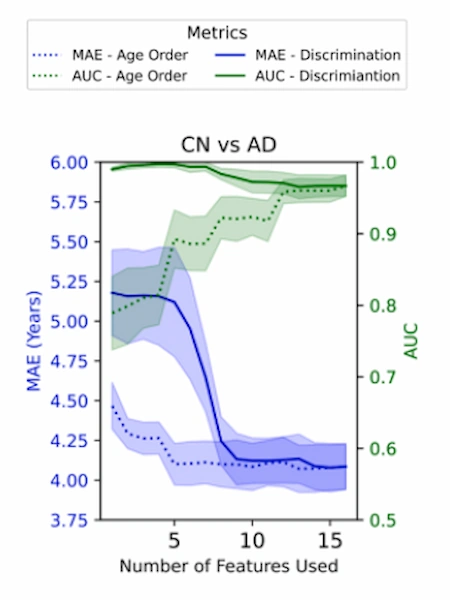
Este resultado sugiere que los cambios asociados al envejecimiento y los cambios asociados al alzhéimer no son exactamente los mismos procesos biológicos.
El papel clave del hipocampo
Entre todas las variables analizadas, el hipocampo destacó como una de las regiones cerebrales más relevantes.
Su volumen mostró una fuerte capacidad para diferenciar entre los distintos grupos clínicos, lo que coincide con la evidencia previa: el hipocampo es una de las primeras estructuras afectadas por la patología de alzhéimer y su atrofia se relaciona estrechamente con los déficits de memoria.
¿Son útiles los modelos BrainAge para diagnosticar alzhéimer?
Los investigadores compararon también dos estrategias diferentes:
- Clasificar a los pacientes utilizando el BrainAge delta.
- Clasificarlos utilizando directamente las variables cerebrales.
Los resultados mostraron que, en muchos casos, usar las variables directamente era igual o incluso más eficaz que utilizar el BrainAge delta.
Esto indica que los modelos BrainAge no siempre aportan información adicional para el diagnóstico.
Sin embargo, presentan una ventaja conceptual importante: generan una única métrica continua, que podría utilizarse como indicador de riesgo o como herramienta para monitorizar la progresión de la enfermedad a lo largo del tiempo.
¿Qué implicaciones tiene para la investigación en alzhéimer?
Este estudio aporta varias conclusiones relevantes para el desarrollo de biomarcadores basados en inteligencia artificial:
- Separar envejecimiento y enfermedad es fundamental. Los modelos que intentan capturar ambos procesos simultáneamente pueden confundir cambios normales del envejecimiento con neurodegeneración.
- La selección de variables es clave. Dependiendo del objetivo —predecir edad o detectar enfermedad— deben utilizarse diferentes tipos de variables.
- Los modelos deben diseñarse para tareas específicas. Un modelo optimizado para estimar edad biológica no necesariamente será el mejor para diagnosticar alzhéimer.
En definitiva, el envejecimiento no es simplemente el “ruido” de fondo en la enfermedad de Alzheimer, sino un proceso que interactúa activamente con la patología.
¿Cómo se relaciona este avance con NeuronUP?
Comprender mejor la diferencia entre envejecimiento cerebral y deterioro neurodegenerativo tiene implicaciones directas para la rehabilitación cognitiva.
En plataformas como NeuronUP, utilizadas para el entrenamiento cognitivo y la estimulación de funciones ejecutivas, memoria o atención, disponer de biomarcadores fiables puede ayudar a:
- identificar pacientes en fases tempranas.
- personalizar programas de rehabilitación según el perfil cognitivo.
- monitorizar la evolución de los pacientes a lo largo del tiempo.
Mientras que herramientas como BrainAge contribuyen a mejorar la detección y comprensión de la enfermedad, soluciones digitales como NeuronUP permiten intervenir sobre el funcionamiento cognitivo y la calidad de vida de los pacientes.
Este estudio ha sido liderado por el Dr. Jesus M. Cortes, quien es también Director de Investigación en NeuronUP, desde el Instituto de Investigación Sanitaria BioBizkaia y en colaboración con investigadores en Harvard Medical School, University Carlos III de Madrid, Vrije Universiteit Amsterdam, Brigham & Women’s, University of Melbourne, Ikerbasque y la Universidad del País Vasco.
Conclusiones para profesionales
Los modelos BrainAge representan una herramienta prometedora para estudiar el envejecimiento cerebral y su relación con la enfermedad de Alzheimer. Sin embargo, este estudio demuestra que la relación entre edad cerebral y neurodegeneración es compleja.
Las variables estructurales del cerebro son especialmente útiles para estimar la edad biológica, mientras que las pruebas cognitivas resultan más eficaces para distinguir entre diferentes estados clínicos.
Por ello, el desarrollo de modelos predictivos en alzhéimer debe tener en cuenta qué proceso se quiere estudiar —envejecimiento o enfermedad— y seleccionar cuidadosamente las variables utilizadas.
En el futuro, integrar biomarcadores biológicos, neuroimagen y herramientas digitales de evaluación y rehabilitación cognitiva podría ofrecer una visión más completa y personalizada del tratamiento del alzhéimer.
Bibliografía
- Garcia Condado J, Verdugo Recuero I, Tellaetxe-Elorriaga I, Birkenbihl C, Carrigan M, Diez I, Buckley RF, Erramuzpe A, Cortes JM. Aging as an active player in Alzheimer’s disease classification: Insights from feature selection in BrainAge models. NeuroImage. 2025. doi:10.1016/j.neuroimage.2025.121548.
Preguntas frecuentes sobre edad cerebral (BrainAge) y alzhéimer
1. ¿Qué es el BrainAge Delta y cómo ayuda a detectar el envejecimiento acelerado?
El BrainAge Delta es la diferencia métrica entre la edad biológica del cerebro (estimada por IA) y la edad cronológica del paciente.
- Valor positivo: Indica un cerebro que parece «más viejo» de lo esperado, lo cual es una señal de alerta temprana de deterioro neurológico.
- Valor negativo: Sugiere un cerebro «más joven», lo que suele asociarse a una mejor reserva cognitiva.
En centros de neurorrehabilitación, esta métrica permite monitorizar objetivamente el riesgo de progresión del paciente.
2. ¿Es la edad cerebral suficiente para diagnosticar el alzhéimer en clínica?
No por sí sola. Según la investigación liderada por el Instituto de Investigación Sanitaria Biobizkaia, existe un «compromiso» (trade-off) entre la precisión al predecir la edad y la capacidad para diagnosticar la enfermedad.
Los modelos que mejor estiman la edad no siempre son los más eficaces para distinguir entre un cerebro sano y uno con alzhéimer. De hecho, usar directamente las variables cerebrales puede ser igual o más eficaz que el cálculo del BrainAge Delta para el diagnóstico clínico.
3. ¿Qué variables discriminan mejor la enfermedad de Alzheimer: la neuroimagen o los test cognitivos?
El estudio demuestra que la elección de la herramienta depende del objetivo clínico:
- Neuroimagen (Resonancia Magnética T1): Es la más informativa para predecir la edad cerebral y captar el envejecimiento natural.
- Pruebas Neuropsicológicas (MMSE, MoCA, ADAS): Son significativamente más eficaces para discriminar clínicamente entre pacientes sanos, con deterioro cognitivo leve (MCI) y Alzheimer.
Esto confirma que el rendimiento cognitivo refleja mejor las diferencias patológicas que la estructura cerebral aislada.
4. ¿Por qué el hipocampo es clave en los modelos de BrainAge?
El volumen del hipocampo destaca como una de las regiones más relevantes por su dualidad:
- Es fundamental para estimar la edad biológica.
- Posee una fuerte capacidad para diferenciar grupos clínicos debido a que es una de las primeras estructuras afectadas por la atrofia en el Alzheimer.
Su análisis es vital para cualquier programa de estimulación cognitiva centrado en la memoria.
6. ¿Qué implicaciones tienen estos hallazgos para la rehabilitación cognitiva?
Comprender la interacción entre envejecimiento y patología permite a los profesionales en España y Latinoamérica diseñar intervenciones más personalizadas. El uso de biomarcadores digitales y modelos de IA ayuda a:
- Identificar fases tempranas: Detectar pacientes antes de que el deterioro sea evidente.
- Personalizar programas: Ajustar la estimulación de funciones ejecutivas y atención en plataformas como NeuronUP según el perfil biológico del usuario.
- Seguimiento preciso: Evaluar el impacto de la rehabilitación en la «salud cerebral» a lo largo del tiempo.
7. ¿Por qué es importante separar envejecimiento y enfermedad en Alzheimer?
Porque mezclar ambos procesos puede llevar a interpretaciones erróneas. El estudio demuestra que los modelos BrainAge pueden captar envejecimiento normal, por lo que es fundamental seleccionar bien las variables según el objetivo clínico.






 Neurociencia del dolor crónico: cómo la terapia de reversión del dolor (TRD) reentrena el cerebro
Neurociencia del dolor crónico: cómo la terapia de reversión del dolor (TRD) reentrena el cerebro 
Deja una respuesta